题目内容
7.化学上通常用AZX来表示一种原子的组成.其中X为元素符号,Z为核电荷数,A为相对原子质量(相对原子质量≈质量数).现有126C、136C 两种粒子 回答:(1)它们是否属于同一种元素?为什么?
(2)比较这两种原子的不同点.
分析 利用题干中的信息对三种碳原子的结构进行分析,再利用原子中的一些等量关系进行求解判断即可;
在原子中,核电荷数=质子数=核外电子数,相对原子质量=质子数+中子数,决定元素种类的微粒是质子数或核电荷数;
解答 解:由题干的信息进行分析可知
126C、136C 两种粒子的质子数(核电荷数)相同都是6,由于三者具有相同的质子数可判断它们是同种元素.126C、136C 两种粒子的相对原子质量分别是12、13,而原子中相对原子质量=质子数+中子数,由于其核电荷数相同都是6,所以其中子数一定不同.而原子中质子数等于核外电子数,所以三者的电子数一定相同.故其最外层电子数也一定相同,因此其化学性质相同;
故答案为:(1)是;126C、136C 两种粒子的质子数(核电荷数)相同都是6;(2)相对原子质量不同,中子数一定不同.
点评 此题是对原子结构的考查,解题的关键是利用题干分析出三种原子的结构,要熟记规律“在原子中,核内质子数=核外电子数=核电荷数,相对原子质量=质子数+中子数”.

练习册系列答案
相关题目
17.下面是某同学进行碱的化学性质实验时记录的实验现象,其中与事实不相符的是( )
| A. | 在Ca(OH)2溶液中加入稀盐酸,无明显变化 | |
| B. | 在NaOH溶液中通入CO2气体,有白色沉淀生成 | |
| C. | 在Ca(OH)2溶液中加入几滴石蕊溶液,溶液呈蓝色 | |
| D. | 在NaOH溶液中加入FeCl3溶液,有红褐色沉淀生成 |
15.20℃时,氯化钠的溶解度为36g.对这句话理解正确的是( )
| A. | 20℃时,100g水中能溶解氯化钠36g,形成136克氯化钠的饱和溶液 | |
| B. | 20℃时,100g氯化钠饱和溶液中含氯化钠36g | |
| C. | 20℃时,氯化钠饱和溶液中水与氯化钠的质量比为64:36 | |
| D. | 20℃时,将36g氯化钠溶解于64g水中,所得溶液为该温度下氯化钠的饱和溶液 |
12.现实生活中,氨气多用作致冷剂及农用化肥,其实它还是一种清洁能源,在纯氧中可以完全燃烧,只生成水和氮气.最近,科学家用一种含钼的化合物作催化剂,在常温下就能完成氨的合成,从而大大降低了生产成本,使得液氨有望取代液氢成为新一代绿色能源.
(1)N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3,该反应属于基本反应类型中的化合反应.
(2)写出氨气在氧气中燃烧的化学方程式4NH3+3O$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
(3)请你根据下表信息分析用NH3取代H2的优点:
①由于NH3比H2沸点高,所以更易液化,便于储存和运输.
②NH3泄漏时易发现是因为有刺激性气味,一旦泄漏,可用水雾冲洗处理.
(1)N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3,该反应属于基本反应类型中的化合反应.
(2)写出氨气在氧气中燃烧的化学方程式4NH3+3O$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
(3)请你根据下表信息分析用NH3取代H2的优点:
| 名称 | 颜色、气味 | 熔点(℃) | 沸点(℃) | 25℃水中溶解度(g/L) | 标况下密度 (g/L) |
| NH3 | 无色、刺激性 | -77.7 | -33 | 456 | 0.6942 |
| H2 | 无色、无味 | -259.2 | -253 | 0.0015 | 0.0899 |
②NH3泄漏时易发现是因为有刺激性气味,一旦泄漏,可用水雾冲洗处理.
19.用如图装置电解水,一段时间后的现象如图所示.对该实验的描述错误的是( )
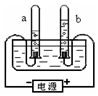

| A. | a试管中收集到的是一种可燃性气体 | |
| B. | 该实验能证明水是由氢元素和氧元素组成 | |
| C. | b试管中收集到的是氧气 | |
| D. | a、b两试管内收集到的气体的质量比约为2:1 |
16.已知SO2与 CO2有许多化学性质是相似的,亚硫酸钙(CaSO3)是白色难溶于水但可溶于酸的固体.某同学向一酸雨样品中滴加 CaCl2,溶液本观察到有浑浊现象,继续滴入NaOH溶液后即有白色沉淀产生.在以上实验过程中,下列不可能发生的化学反应是( )
| A. | SO2+CaCl2+H2O═CaSO3↓十2HCl | B. | SO2+2NaOH═Na2SO3+H2O | ||
| C. | Na2SO3+CaCl2=CaSO3↓+2NaCl | D. | H2SO3+2NaOH=Na2SO3+2H2O |
17.下列各组溶液中,不用其它任何试剂就能鉴别出来的是( )
| A. | FeCl3 NaOH HCl KCl | |
| B. | BaCl2 Na2SO4 NaOH HCl | |
| C. | CuSO4 NaCl KNO3 BaCl2 | |
| D. | KCl AgNO3 HCl HNO3 |
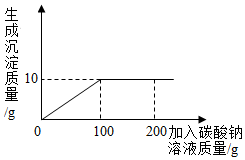 为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:取14克固体样品,全部溶于100克水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录并绘制了如图所示的曲线
为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:取14克固体样品,全部溶于100克水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录并绘制了如图所示的曲线