题目内容
11.加热31.6g高锰酸钾,一段时间后,冷却,测得剩余固体中钾元素的质量分数为26%,则生成氧气的质量为( )| A. | 1.6 g | B. | 0.8 g | C. | 2.4 g | D. | 3.2 g |
分析 根据高锰酸去钾加热生成锰酸钾、二氧化锰和氧气,根据质量守恒定律可知反应前后剩余固体中钾元素的质量不改变,剩余固体的质量减小且减小的质量就是生成的氧气的质量;所以求出高锰酸钾中钾元素的质量分数,然后用高锰酸钾的质量乘以这个数求出反应前钾元素的质量,用钾元素的质量除以剩余物中钾元素的质量分数求出剩余固体的质量,31.6g减去这个质量就是生成的氧气的质量.
解答 解:KMnO4中钾元素的质量分数为:$\frac{39}{158}$×100%=24.7%,高锰酸钾中钾元素的质量为31.6g×24.7%=7.8g,剩余固体的质量为$\frac{7.8g}{26%}$=30g,生成的氧气的质量为31.6g-30g=1.6g.
故选A.
点评 本题主要理清反应前后钾元素的质量不变,再根据化学式求解即可.

练习册系列答案
相关题目
6.如图是元素周期表中的一种元素,下列有关该元素的信息不正确的是( )


| A. | 原子序数是13 | B. | 它是非金属元素 | ||
| C. | 元素符号为Al | D. | 相对原子质量是26.98 |
3.下列实验操作正确的是( )
| A. | 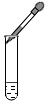 | B. |  | C. | 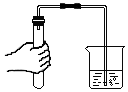 | D. | 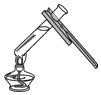 |
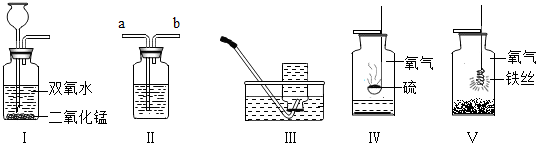

 酸碱盐是有广泛用途的重要化合物,某化学活动小组的同学围绕这几类化物合进行了一系探究活动.
酸碱盐是有广泛用途的重要化合物,某化学活动小组的同学围绕这几类化物合进行了一系探究活动.