题目内容
18.物质的用途和使用方法等于其性质密切相关.(1)铁粉常用于食品的保鲜剂,其原因是铁粉与水和氧气反应.
(2)生石灰常用作食品干燥剂,用化学方程式表示其原因是CaO+H2O=Ca(OH)2.
(3)浓硫酸是无色粘稠液体,有吸水性,在化学实验中常用它作干燥剂,但日常生活中却很少用它作除湿剂,原因是浓硫酸具有很强的腐蚀性.
分析 (1)根据食品在与氧气接触时容易发生缓慢氧化而变质,铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果进行分析;
(2)根据氧化钙和水会生成氢氧化钙进行分析;
(3)根据浓硫酸的性质进行分析.
解答 解:(1)食品在与氧气接触时容易发生缓慢氧化而变质,铁粉能吸收空气中的氧气和水蒸气,从而延长保质期,常用于食品的保鲜剂;
(2)生石灰与水反应生成氢氧化钙,可作干燥剂,化学方程式为:CaO+H2O=Ca(OH)2;
(3)浓硫酸是无色粘稠液体,有吸水性,在化学实验中常用它作干燥剂,但日常生活中却很少用它作除湿剂,原因是:浓硫酸具有很强的腐蚀性.
故答案为:(1)铁粉与水和氧气反应;
(2)CaO+H2O═Ca(OH)2;
(3)浓硫酸具有很强的腐蚀性.
点评 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的;对于化学方程式的考查始终是中考的热点.

练习册系列答案
相关题目
8.现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
求:
(1)该混合物粉末中铜的质量分数52.5%;
(2)若参加反应的金属为R,请写出R与稀硫酸反应的化学方程式R+H2SO4═RSO4+H2↑;
(3)设金属R的相对原子质量为X,根据已知条件列出求解(X)的比例式$\frac{X}{98}=\frac{1.2g}{4.9g}$;
(4)如果将第三次加入硫酸充分反应后的溶液蒸发掉8.3g水,且无晶体析出,则所得溶液中溶质的质量分数为18.0%.
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物粉末中铜的质量分数52.5%;
(2)若参加反应的金属为R,请写出R与稀硫酸反应的化学方程式R+H2SO4═RSO4+H2↑;
(3)设金属R的相对原子质量为X,根据已知条件列出求解(X)的比例式$\frac{X}{98}=\frac{1.2g}{4.9g}$;
(4)如果将第三次加入硫酸充分反应后的溶液蒸发掉8.3g水,且无晶体析出,则所得溶液中溶质的质量分数为18.0%.
9.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表,下列说法中不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
| A. | 该反应为分解反应 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 该反应中甲、乙两种物质间的质量比为1:4 | |
| D. | 乙中含有两种或两种以上元素 |
13.下列四个图象中,能正确反映对应变化关系的是( )
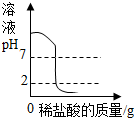 | 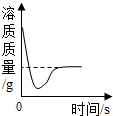 | 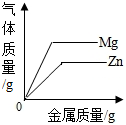 | 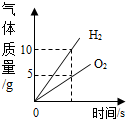 |
| A.向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量 | B.某温度时,向一定量的饱和石灰水中加入少量生石灰 | C.向两份完全相同的稀盐酸中分别加入足量的锌粉、镁粉 | D.将水通电一段时间 |
| A. | A | B. | B | C. | C | D. | D |
3.同学们运用对比的学习方法探究碱的性质.
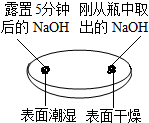
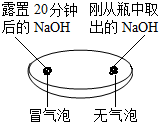
(1)由实验一、二可知,氢氧化钠会吸收空气中的二氧化碳和水,因此要密封保存.
(2)实验三种观察到3个塑料瓶变瘪的程度为A>B>C,对此A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠和氢氧化钙两种饱和溶液.
(4)某同学发现工业上使用的氢氧化钠固体标签如图所示,于是对其成分进行了探究:

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】①在华工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.
提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过滤稀盐酸.
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中含有氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
| 实验一 观察固体表面 | 实验二 向两块固体表面滴加稀盐酸 | 实验三 振荡3个塑料瓶 |
 |  |  |
(2)实验三种观察到3个塑料瓶变瘪的程度为A>B>C,对此A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠和氢氧化钙两种饱和溶液.
| 实验一 | 实验二 | 分析 |
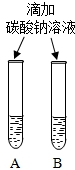 | 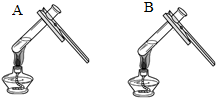 微热(不考虑水分蒸发) | 两种方案中均观察到A试管内出现白色浑浊,则A中溶液为饱和氢氧化钙溶液;方案二的设计原理是氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大. |

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】①在华工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.
提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过滤稀盐酸.
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中含有氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)