题目内容
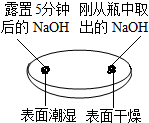
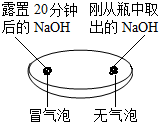
3.同学们运用对比的学习方法探究碱的性质.| 实验一 观察固体表面 | 实验二 向两块固体表面滴加稀盐酸 | 实验三 振荡3个塑料瓶 |
 |  |  |
(2)实验三种观察到3个塑料瓶变瘪的程度为A>B>C,对此A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠和氢氧化钙两种饱和溶液.
| 实验一 | 实验二 | 分析 |
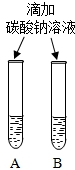 | 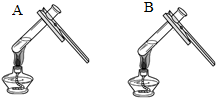 微热(不考虑水分蒸发) | 两种方案中均观察到A试管内出现白色浑浊,则A中溶液为饱和氢氧化钙溶液;方案二的设计原理是氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大. |

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】①在华工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.
提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过滤稀盐酸.
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中含有氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
分析 (1)根据氢氧化钠的化学性质进行分析;
(2)根据二氧化碳与氢氧化钠、氢氧化钙、水的反应;
(3)根据氢氧化钠与氢氧化钙的溶解性进行分析;
(4)【提出猜想】根据氢氧化钠的制法和变质进行分析;
【反思评价】②根据氢氧根离子验证进行分析;
(5)①分析反应可发现,反应前为碳酸钠和氯化钠的混合物,而反应后得到固体为氯化钠,质量增加了12.1g-11g=1.1g,而该过程中是固体的质量增加了,所以可以根据差量法进行解答;
②反应后溶液的质量为反应前样品的质量+稀盐酸的质量-生成的二氧化碳的质量,然后结合溶液中溶质的质量分数的计算公式进行计算即可.
解答 解:(1)由上图实验一、二可知,氢氧化钠会吸收空气的 H2O、CO2,因此要密封保存;
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶内发生反应为二氧化碳与氢氧化钠溶液反应,对比A瓶与C瓶的实验现象可证明CO2能与NaOH发生反应;
(3)考虑氢氧化钠与氢氧化钙的溶解性:两种方案中均观察到A试管内出现白色浑浊,A中试剂为饱和氢氧化钙溶液;方案二的设计原理是利用了氢氧化钙的溶解度随温度升高而减少;氢氧化钠的溶解度随温度升高而升高;两者的溶解度受温度影响情况不同;
| 实验一 | 实验二 | 分析 |
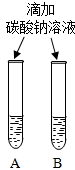 | 微热(不考虑水分蒸发)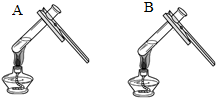 | 两种方案中均观察到A试管内出现白色浑浊,则A中溶液为饱和氢氧化钙溶液;方案二的设计原理是氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大 |
【反思评价】②要验证氢氧化钠,首先要排除碳酸钠的干扰,可以取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠;
(5)解:设碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x $\frac{73x}{106}$ $\frac{117x}{106}$ $\frac{44x}{106}$
则11g-x+$\frac{117x}{106}$=12.1g
解得:x=10.6g
②反应后所得溶液中溶质的质量分数为:$\frac{12.1g}{11g+7.3g+14.6g-4.4g}$×100%≈21.4%
答:①碳酸钠样品中碳酸钠的质量为10.6g;
②反应后所得溶液中溶质的质量分数为21.4%.
故答案为:(1)二氧化碳和水;
(2)C;
(3)饱和氢氧化钙溶液;氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大;
| 实验一 | 实验二 | 分析 |
| 饱和氢氧化钙溶液;氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大 |
【反思评价】②取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠;
(5)①碳酸钠样品中碳酸钠的质量为10.6g;
②反应后所得溶液中溶质的质量分数为21.4%.
点评 熟练掌握二氧化碳和氢氧化钠、氢氧化钙的化学性质,能够根据物质的性质设计实验对物质进行鉴别,在学习中要注意培养自己设计实验的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列说法正确的是( )
| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 有机物都是含碳的化合物,CO、CO2也是有机物 | |
| C. | 化学纤维和羊毛可以用燃烧法区别 | |
| D. | 生物微量元素是人体必需的营养素,多吃无害 |
11.下列有关空气成分的说法不正确的是( )
| A. | 空气中氧气的体积分数约为21% | |
| B. | 惰性气体一般不跟其他物质发生反应 | |
| C. | 二氧化碳含量上升不会影响环境 | |
| D. | 敞口放置的饼干变软与水蒸气有关 |
8.下列物质:①空气、②硫酸、③氧气、④硫酸钠、⑤水、⑥氢氧化钠、⑦天然气、⑧生铁、⑨碳酸钙,对其分类完全正确的一组是( )
| A. | 盐:④⑨ | B. | 酸:②④ | C. | 氧化物:③⑤ | D. | 混合物:①⑥⑦⑧ |
15.下列化学用语错误的是( )
| A. | 2个氮原子:2N | |
| B. | 三氧化二铝中铝元素的化合价:${\;}_{A{l}_{2}{O}_{3}}^{+3}$ | |
| C. | 2个钠离子:2Na- | |
| D. | 一个水分子:H2O |
 尿素是一种农业上常用的高效氮肥,它的化学式为CO(NH2)2.
尿素是一种农业上常用的高效氮肥,它的化学式为CO(NH2)2.