题目内容
17.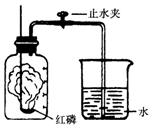 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并作好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)红磷燃烧的现象是冒出大量的白烟,放出热量.
(2)该实验中红磷需稍过量,目的是将集气瓶内的氧气消耗尽.
(3)步骤③中打开止水夹后观察到的现象是烧杯中的水倒流至集气瓶,液面上升在一等分刻度处由此可得出空气中氧气的体积约为空气体积的$\frac{1}{5}$.
(4)该实验可推论出氮气难(填“易”或“难”)溶于水和其化学性质不活泼(填“活泼”或“不活泼”)的结论.
分析 (1)根据红磷的燃烧现象来分析解答;
(2)根据该实验注意事项分析;
(3)根据红磷与氧气反应生成五氧化二磷固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶;
(4)根据集气瓶内剩余的气体主要是氮气分析氮气的性质.
解答 解:(1)点燃的红磷,在集气瓶燃烧,生成大量的白烟,放出热量;故填:冒出大量的白烟,放出热量.
(2)该实验中红磷需稍过量,目的是:确保将集气瓶内的氧气消耗尽;故填:将集气瓶内的氧气消耗尽;
(3)由于红磷与氧气反应生成五氧化二磷固体,消耗了瓶内的气体,压强减小,所以,打开止水夹后观察到的现是:烧杯中的水倒流至集气瓶,液面上升在一等分刻度处,说明氧气约占空气体积的五分之一;故填:烧杯中的水倒流至集气瓶;液面上升在一等分刻度处;$\frac{1}{5}$;
(4)由于集气瓶内剩余的气体主要是氮气,由此可知氮气的性质是难溶于水、不能燃烧也不能支持燃烧,即化学性质不活泼;故填:难;不活泼.
点评 本题能通过实验探究的方式考查了氧气含量的测定,熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.

练习册系列答案
相关题目
8. 如图是元素周期表中的两种元素的部分信息,(a)、(b)对应为这两种元素的粒子结构示意图,所获得的信息正确的是( )
如图是元素周期表中的两种元素的部分信息,(a)、(b)对应为这两种元素的粒子结构示意图,所获得的信息正确的是( )
 如图是元素周期表中的两种元素的部分信息,(a)、(b)对应为这两种元素的粒子结构示意图,所获得的信息正确的是( )
如图是元素周期表中的两种元素的部分信息,(a)、(b)对应为这两种元素的粒子结构示意图,所获得的信息正确的是( )| A. | Z处元素的符号是Cl | |
| B. | 两种元素的化学性质相似,都属于非金属元素 | |
| C. | Y处元素的名称是钠,(a)中X处质子数为11 | |
| D. | (b)表示的阴离子的符号是Cl-,氯元素的相对原子质量是35.45g |
12.一种氟原子的原子核内有9个质子和10个中子,该原子的核电荷数为( )
| A. | 7 | B. | 10 | C. | 9 | D. | 19 |
9.能反映相关实验过程中量的变化的图象是( )
| A. |  用一氧化碳还原氧化铁 | |
| B. |  向盛有一定量的氢氧化钠溶液的烧杯中逐滴加入pH=2的稀盐酸至过量 | |
| C. |  相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应 | |
| D. |  等质量、等质量分数的双氧水完全分解 |
