题目内容
7.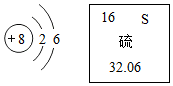 如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息.下列说法正确的是( )
如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息.下列说法正确的是( )| A. | 氧原子核外有6个电子 | |
| B. | 硫、氧均属于非金属元素 | |
| C. | 硫原子的相对原子质量为32.06g | |
| D. | 硫、氧两种元素形成的SO3中硫元素为+4价 |
分析 A、根据在原子中,质子数=核外电子数解答;
B、根据硫、氧均属于非金属元素解答;
C、根据相对原子质量的单位来分析;
D、根据化合物中元素化合价的代数和为0解答.
解答 解:
A、在原子中,质子数=核外电子数,由结构示意图可知:氧原子核外有8个电子,故错误;
B、硫、氧均属于非金属元素,故正确;
C、相对原子质量的单位是“1”而不是“g”,硫原子的相对原子质量为32.06,故错误;
D、硫、氧两种元素形成的SO3中硫元素为x,则x+(-2)×3=0,x=+6,故错误.
答案:B
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子结构示意图的意义进行分析解题的能力.

练习册系列答案
相关题目
15.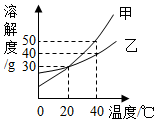 如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
 如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )| A. | 20℃时,甲、乙两种固体物质的溶解度都是30 | |
| B. | 40℃时,甲的饱和溶液中溶质质量分数为50% | |
| C. | 40℃时,将50g乙物质全部溶于水中,恰好能得到150g乙的饱和溶液 | |
| D. | 将130g20℃甲的饱和溶液升温到40℃,最多还能溶解甲物质20g |
12.下列科学家与他的贡献对应不正确的是( )
| A. | 侯德榜---联合制碱法 | |
| B. | 门捷列夫---元素周期表 | |
| C. | 阿基米德---杠杆原理:F1l1=F2l2 | |
| D. | 欧姆---电流通过导体产生的热量:Q=I2Rt |
19.下列对分子、原子、离子的认识,正确的是( )
| A. | 分子是保持物质性质的一种粒子 | B. | 原子是最小的粒子,不可再分 | ||
| C. | 温度越高,分子运动速率越快 | D. | 铝原子与铝离子的化学性质相同 |






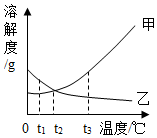 图为甲、乙两种固体物质在水中的溶解度曲线.
图为甲、乙两种固体物质在水中的溶解度曲线.