题目内容
16.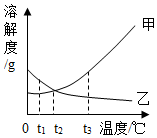 图为甲、乙两种固体物质在水中的溶解度曲线.
图为甲、乙两种固体物质在水中的溶解度曲线.(1)当温度为t2℃时,甲乙两种固体物质的溶解度相等.
(2)把t3℃的甲乙两种物质的饱和溶液降温到t1℃,乙溶液变为不饱和溶液.
(3)若甲种混有少量乙物质,提纯甲常采用的方法是降温结晶.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,当温度为t2℃时,甲、乙两种固体物质的溶解度相等;
(2)乙物质的溶解度随温度的降低而增大,所以把t3℃的甲乙两种物质的饱和溶液降温到t1℃,乙溶液变为不饱和溶液;
(3)甲物质的溶解度受温度变化影响较大,所以甲种混有少量乙物质,提纯甲常采用的方法是降温结晶.
故答案为:(1)相等;
(2)乙;
(3)降温结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
6.推理是学习化学的一种重要方法,但推理必须科学、严谨.下列推理正确的是( )
| A. | 木炭在氧气中能燃烧,所以氧气具有可燃性 | |
| B. | 不锈钢虽然是金属材料,但它属于混合物而不是金属单质 | |
| C. | 原子核是由质子和中子构成的,故所有原子核中都一定含有质子和中子 | |
| D. | 催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂 |
7.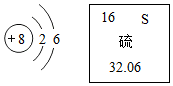 如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息.下列说法正确的是( )
如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息.下列说法正确的是( )
 如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息.下列说法正确的是( )
如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息.下列说法正确的是( )| A. | 氧原子核外有6个电子 | |
| B. | 硫、氧均属于非金属元素 | |
| C. | 硫原子的相对原子质量为32.06g | |
| D. | 硫、氧两种元素形成的SO3中硫元素为+4价 |
4.雄伟壮丽的国家大剧院主体建筑表面安装了2万多块钛(Ti)合金板,已知钛原子核内有22个质子,则下列叙述正确的是( )
| A. | TiO2中含有氧分子 | B. | Ti可以表示一个钛原子 | ||
| C. | Ti4+核外有26个电子 | D. | CaTiO3属于金属氧化物 |
11.下列离子能在pH=13的溶液中大量共存的是( )
| A. | Mg2+ Cl- Cu2+ NO3- | B. | H+ CO32- K+ SO42- | ||
| C. | Ba2+ Cl- NO3- Na+ | D. | NH4+ HCO3- Al3+ SO42- |
3.下列叙述对应的图象正确的是( )
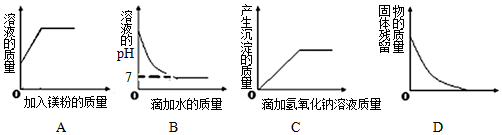

| A. | 向一定质量的硫酸铜溶液中加镁粉至过量 | |
| B. | 向一定质量的稀盐酸中滴加水 | |
| C. | 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液至过量 | |
| D. | 加热一定质量的碳酸氢铵 |
10.硬水中含有较多的可溶性钙和镁的化合物,加热时易分解为CaCO3等难溶物质而形成水垢,因此会给生活和生产带来许多影响.敏敏通过查找资料得知:大多数碳酸盐难溶于水,但雨水、河水中溶有CO2后,就会与土壤、岩石中的CaCO3、MgCO3等反应生成可溶性的碳酸氢盐进入水中,绝大多数碳酸盐都具有类似的性质.即:CaCO3+H2O+CO2═Ca(HCO3)2,Ca(HCO3)2$\frac{\underline{\;加热\;}}{\;}$CaCO3↓+H2O+CO2↑.请你结合所学知识分析,下列说法中不正确的是( )
| A. | 向澄清的石灰水中不断地通入CO2,最终一定会有白色沉淀产生 | |
| B. | 可用加热的方法除去碳酸钠固体中混有的少量碳酸氢钠 | |
| C. | 除去CO2中的HCl气体,用饱和碳酸氢钠溶液 | |
| D. | 已知相同条件下,碳酸氢钠的溶解度远小于碳酸钠的溶解度.在一定温度下,向一定量的饱和碳酸钠溶液中通入足量的CO2,有沉淀析出 |
7.下列符号中,既可以表示一个原子,又可以表示一种元素,还能表示一种物质的是( )
| A. | Cl | B. | Hg | C. | N | D. | H2 |