题目内容
5.下列对实验现象的描述正确的是( )| A. | 镁条在空气中剧烈燃烧,发出耀眼白光,生成白色固体 | |
| B. | 铁锈在稀盐酸里浸泡一段时间后,铁锈消失,溶液变为浅绿色 | |
| C. | 向淀粉溶液中滴加碘水,溶液变为蓝色 | |
| D. | 向硫酸铜溶液中滴加氢氧化钠溶液,生成白色沉淀 |
分析 A、根据镁条在空气中燃烧的现象,进行分析判断.
B、根据酸的化学性质,进行分析判断.
C、根据碘遇淀粉变蓝色的特性,进行分析判断.
D、根据碱的化学性质,进行分析判断.
解答 解:A、镁条在空气中剧烈燃烧,发出耀眼白光,生成白色固体,故选项说法正确.
B、铁锈在稀盐酸里浸泡一段时间后,氧化铁与稀盐酸反应生成氯化铁和水,铁锈消失,溶液变为黄色,故选项说法错误.
C、碘遇淀粉变蓝色,向淀粉溶液中滴加碘水,溶液变为蓝色,故选项说法正确.
D、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,氢氧化钠溶液加入硫酸铜溶液中产生蓝色沉淀,故选项说法错误.
故选:AC.
点评 本题难度不大,掌握碱的化学性质、酸的化学性质、碘遇淀粉变蓝色等是正确解答本题的关键;在描述实验现象时,应注意生成沉淀的颜色.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.三种金属X、Y、Z及化合物间发生如下化学反应 X+YCl2═Y+XCl2,Z+YCl2═Y+ZCl2
Z+2HCl═ZCl2+H2↑,X与稀盐酸不反应,则X、Y、Z三种金属的活动性由强到弱的顺序是( )
Z+2HCl═ZCl2+H2↑,X与稀盐酸不反应,则X、Y、Z三种金属的活动性由强到弱的顺序是( )
| A. | Z>Y>X | B. | Z>X>Y | C. | X>Y>Z | D. | Y>Z>X |
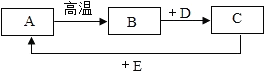 A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,是一种常见的干燥剂,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).
A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,是一种常见的干燥剂,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).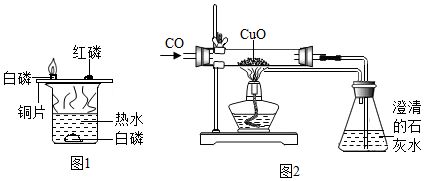

 A~F和X、Y都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如图所示:
A~F和X、Y都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如图所示: