题目内容
1.加热氯酸钾和二氧化锰的混合物60克至完全反应,固体质量变为40.8克,反应后的固体物质是什么?质量分别为多少克?分析 根据质量守恒定律计算生成氧气的质量,然后依据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,结合氧气的质量计算氯化钾的质量,计算参加反应的氯酸钾的质量,然后计算未参加反应的氯酸钾质量.
解答 解:生成氧气的质量为:60g-40.8g=19.2g,
设生成氯化钾的质量为y,参加反应的氯酸钾质量为z
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 149 96
z y 19.2g
$\frac{245}{z}$=$\frac{149}{y}$=$\frac{96}{19.2g}$
y=29.8g
z=49g
所以二氧化锰质量为:60g-49g=11g.
答:反应后的固体物质是氯化钾和二氧化锰,质量分别是:29.8g,11g.
点评 解答此类题的方法是:首先利用质量守恒定律,根据反应前后固体物质质量差求得反应生成气体的质量;然后,利用化学方程式由气体质量计算其他物质的质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下面是一些物质的自我介绍,其中介绍化学性质的是( )
| A. | 镁--“我是银白色” | B. | 一氧化碳--“我可燃烧” | ||
| C. | 氢气--“我是最轻的气体” | D. | 金刚石--“我是最硬的矿物” |
16.化学反应前后,下列各项一定不发生改变的是( )
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类 ⑦原子的质量
⑧物质的总质量.
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类 ⑦原子的质量
⑧物质的总质量.
| A. | ①②⑤⑦⑧ | B. | ①②③⑦ | C. | ⑤⑥⑧ | D. | ①②⑤⑥⑦⑧ |
13.图为水通电分解的实验装置图,下列说法中正确的是( )


| A. | B试管中产生的气体的化学式是氢气 | |
| B. | 电池的正极与试管A中的电极相连 | |
| C. | A管和B管所产生气体的质量比是2:1 | |
| D. | 水通直流电能分解生成氢气和氧气,说明水是由氢、氧两种元素组成 |
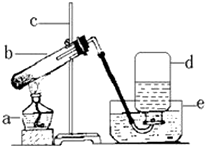 如图为实验室用加热高锰酸钾的方法制取氧气的装置图,回答问题:
如图为实验室用加热高锰酸钾的方法制取氧气的装置图,回答问题: