题目内容
19.有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4中的一种或多种物质组成,小明为了探究其成分,设计并完成了如图所示的实验.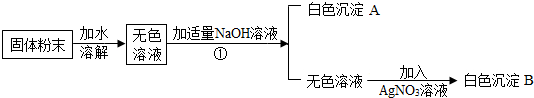
根据以上实验,回答:
(1)请写出操作①的名称过滤.
(2)原固体粉末中一定不含有什么物质?硫酸铜.
(3)请写出生成沉淀A的化学方程式MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
分析 根据硫酸铜在溶液中显蓝色,氯化镁和氢氧化钠反应会生成白色的氢氧化镁沉淀,氯离子和银离子反应会生成白色的氯化银沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,氯化镁和氢氧化钠反应会生成白色的氢氧化镁沉淀,氯离子和银离子反应会生成白色的氯化银沉淀,所以
固体粉末加水溶解,得到无色溶液,白色粉末中一定不含硫酸铜,无色溶液中加入氢氧化钠生成白色沉淀A,固体粉末中一定含有氯化镁,无色溶液中加入硝酸银会生成白色沉淀B,所以B是氯化银沉淀,氯化镁中也会提供氯离子,所以不能确定固体粉末中是否含有氯化钠,题中的现象也不能确定是否含有硝酸钠,所以
(1)操作①的名称过滤;
(2)原固体粉末中一定不含硫酸铜;
(3)生成沉淀A的反应是氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
故答案为:(1)过滤;
(2)硫酸铜;
(3)MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
5. 已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
 已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )| A. | 溶液中碳元素的质量 | B. | 碳酸钠的质量分数 | ||
| C. | 溶剂的质量 | D. | 溶液中钠元素的质量 |
12.下列归纳和总结完全正确的一组是( )
| A化学与资源 | B化学与生活 |
| ①防止金属腐蚀是保护金属资源的途径之一 ②煤、石油、天然气是可再生能源 ③海洋中蕴藏着丰富的化学资源 | ①用洗涤剂去除油污 ②用镶有金刚石的玻璃刀裁玻璃 ③用生石灰作食品干燥剂 |
| C化学与安全 | D化学与发现 |
| ①炒菜锅着火可以用锅盖盖灭 ②在室内放一盆水能防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 | ①波义耳发现酸碱指示剂 ②拉瓦锡发现元素周期律并编制元素周期表 ③门捷列夫发现空气的组成 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关水的说法正确的是( )
| A. | 水是由氧气与氢气组成的 | |
| B. | 水是一种良好溶剂,能溶解所有物质 | |
| C. | 被污染的水经过过滤就可饮用 | |
| D. | 在标准大气压下,水的沸点是100℃ |
10.如图所示,用恒温蒸发氯化钠溶液来模拟海水晒盐的过程,已知图②中的溶液恰好是氯化钠的饱和溶液,则下列说法错误的是( )


| A. | 由图①到图②,溶液的质量减少 | |
| B. | 由图②到图③,溶质的质量不变 | |
| C. | 由图③到图④,溶液的溶质质量分数不变 | |
| D. | 由图①到图④,氯化钠的溶解度保持不变 |
 A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
A、B、C三种物质的溶解度曲线如图所示,请回答下列问题: