题目内容
14.按下列要求,从烧碱、熟石灰、碳酸氢钠、硝酸钾中选出适当的物质,将其化学式填到相应的横线上:可用于砌砖、抹墙和降低土壤酸性的是Ca(OH)2;固体可作某些气体的干燥剂,具有强腐蚀性的是NaOH;焙制糕点所用的发酵粉的主要成分之一是NaHCO3.
分析 首先根据题意确定物质的化学名称,然后根据书写化学式的方法和步骤写出物质的化学式即可.
解答 解:氢氧化钙溶于水形成石灰浆用于砌砖抹墙,也可改良酸性土壤,化学式为:Ca(OH)2;
氢氧化钠是一种具有强烈的腐蚀性的碱,能吸收水分而潮解,故可作干燥剂,化学式为:NaOH;
碳酸氢钠俗称小苏打,是焙制糕点所用的发酵粉的主要成分之一,其化学式为NaHCO3.
故答案为:Ca(OH)2;NaOH;NaHCO3.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
4.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 酸雨的形成 CO2+H2O═H2CO3 化合反应 | |
| B. | 干粉灭火器的反应原理 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2 分解反应 | |
| C. | 用稀硫酸洗去附着在试管壁上的铜 Cu+H2SO4═CuSO4+H2↑ 置换反应 | |
| D. | 误服用氯化钡后用硫酸镁解毒 BaCl2+MgSO4═MgCl2+BaSO4↓ 复分解反应 |
5.除去下列各物质中的少量杂质,所用方法不可行的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | NaNO3 | Na2CO3 | 加足量稀盐酸,蒸发结晶 |
| B | Cu | Fe | 加足量的稀硫酸,过滤 |
| C | CO2 | CO | 通过灼热的CuO |
| D | CaO | CaCO3 | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
9.通过学习同学们知道酸、碱、盐之间产生复分解反应的条件是:两种化合物相互交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生,某实验小组设计如下实验方案来验证酸、碱、盐之间发生复分解反应的条件.
【实验方案】分别取少量的氢氧化钠溶液、氯化钠溶液、碳酸钠粉末、铁钉和硝酸钡溶液盛于五支洁净的试管中,然后分别加入适量稀硫酸,观察并记录实验现象
【实验记录】
【实验结论】
(1)碳酸钠粉末、铁钉和硝酸钡溶液与稀硫酸发生复分解反应;
(2)氢氧化钠溶液、氯化钠溶液不能与稀硫酸发生复分解反应.
【分析评价】
同学们对该小组的实验方案和结论产生很大异议,请你一起参与分析评价.
(1)实验方案中有一种物质选择的不合理,该物质是铁钉,这种物质与稀硫酸反应的基本反应类型是置换反应;
(2)氢氧化钠溶液与稀硫酸混合虽然没有明显现象,但二者能发生复分解反应,理由是反应后有水生成,该反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O.若证明二者能发生反应,应在加入稀硫酸前向氢氧化钠溶液中滴加少量酚酞溶液.
(3)请你找出一种与稀硫酸反应既生成水又生成沉淀的物质Ba(OH)2(填化学式)
【实验方案】分别取少量的氢氧化钠溶液、氯化钠溶液、碳酸钠粉末、铁钉和硝酸钡溶液盛于五支洁净的试管中,然后分别加入适量稀硫酸,观察并记录实验现象
【实验记录】
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钠粉末 | 铁钉 | 硝酸钡溶液 | |
| 稀硫酸 | 无明显现象 | 无明显现象 | 有气泡产生 | 有气泡产生 | 产生白色沉淀 |
(1)碳酸钠粉末、铁钉和硝酸钡溶液与稀硫酸发生复分解反应;
(2)氢氧化钠溶液、氯化钠溶液不能与稀硫酸发生复分解反应.
【分析评价】
同学们对该小组的实验方案和结论产生很大异议,请你一起参与分析评价.
(1)实验方案中有一种物质选择的不合理,该物质是铁钉,这种物质与稀硫酸反应的基本反应类型是置换反应;
(2)氢氧化钠溶液与稀硫酸混合虽然没有明显现象,但二者能发生复分解反应,理由是反应后有水生成,该反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O.若证明二者能发生反应,应在加入稀硫酸前向氢氧化钠溶液中滴加少量酚酞溶液.
(3)请你找出一种与稀硫酸反应既生成水又生成沉淀的物质Ba(OH)2(填化学式)
4.一杯10℃的硝酸钾溶液,能证明它是饱和溶液的方法是( )
| A. | 蒸发5g水有固体溶质析出 | B. | 加入少许硝酸钾晶体不溶 | ||
| C. | 把溶液降温至0℃有固体溶质析出 | D. | 升高温度能继续溶解晶体 |
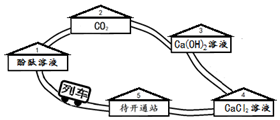 碳酸钠溶液搭乘列车畅游物质世界.如图所示.
碳酸钠溶液搭乘列车畅游物质世界.如图所示.