题目内容
2.某兴趣小组为了研究露置于空气中的纯净生灰石(CaO)的变质情况,进行了如下实验: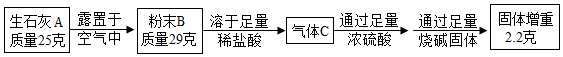
下列结论正确的是( )
| A. | A转化为B过程中钙元素的质量分数逐渐增大 | |
| B. | 若无浓硫酸,则粉末B中CaO质量测定值偏小 | |
| C. | 粉末B中Ca(OH)2质量为5.0 g | |
| D. | A到B中生石灰的变质程度为33.6% |
分析 氧化钙能和空气中的水反应生成氢氧化钙,氢氧化钙能和空气中的二氧化碳反应生成碳酸钙和水,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;根据提供的数据可以进行相关方面的计算.
解答 解:A、根据质量守恒定律,A转化为B过程中钙元素的质量不变,B质量增加,钙元素的质量分数逐渐减小,故错误;
氢氧化钠增加的质量即为二氧化碳的质量,为2.2g;
设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
设这些CaCO3是由质量为y的CaO转化而来,
由CaO+H2 O═Ca(OH)2,Ca(OH)2+CO2═CaCO3↓+H2O可知,CaO~CaCO3,
CaO~CaCO3,
56 100
y 5g
$\frac{56}{y}=\frac{100}{5g}$
y=2.8g
2.8g氧化钙转化成5g碳酸钙后,固体质量增加:5g-2.8g=2.2g,因此氧化钙除部分转化成碳酸钙外,还有一部分转化成氢氧化钙,
设转化成氢氧化钙的质量为z,转化成氢氧化钙的氧化钙的质量为m
CaO+H2 O═Ca(OH)2,固体质量增加
56 74 74-56=18
m z 4g-2.2g=1.8g
$\frac{56}{m}=\frac{74}{z}=\frac{18}{1.8g}$
z=7.4g,m=5.6g
未变质的生石灰的质量为:25g-2.8g-5.6g=16.6g;
B、浓硫酸具有吸水性,如无浓硫酸,氢氧化钠固体质量增加的质量不一定全是二氧化碳的质量,则粉末B中CaO质量测定值偏小,故正确;
C、粉末B中Ca(OH)2的质量为5.6克,故错误;
D、A到B中生石灰的变质程度=$\frac{25g-16.6g}{25g}$×100%=24.3%,故错误.
故选B.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

| A. | 去超市购物,用布袋购物 | |
| B. | 为了卫生,就餐时多使用一次性餐具 | |
| C. | 节约用纸,两面使用 | |
| D. | 节约用电,教室内人走灯灭 |
(1)下面三幅示意图分别表示生成氯化钠的不同化学反应.请根据图示回答相关问题:

①图1是金属钠与氯气反应生成氯化钠的微观示意图.对图1中的有关叙述错误的是C(填序号)
A.元素的化学性质与原子最外层电子数关系密切
B.Na和Na+的化学性质不同
C.NaCl是由氯化钠分子构成的
D.由Cl→Cl-的转变中,元素种类不变
②图2是氢氧化钠与盐酸反应的微观示意图,该反应的实质是A+B→C,请用微粒符号表示该反应的实质H++OH-=H2O.
③图3表示反应中所涉及的4种物质中属于氧化物的是ClO2(填化学式),NaClO2中氯元素的化合价为+3.
(2)稀盐酸、稀硫酸具有相似的化学性质,是因为它们的水溶液中都含有共同的阳离子H+(填离子符号)
(3)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 碳酸氢钠片 | 铝碳酸镁片 |
| 有效成分 | NaHCO3 | AlMg(OH)3CO3 |
| 构成微粒 | Na+、HCO3- | Al3+、Mg2-、OH-、CO32- |
①碳酸氢钠中起抗酸作用的微粒是HCO3-(填微粒符号,下同).
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.则铝碳酸镁中起抗酸作用的两种微粒是OH-、CO32-.
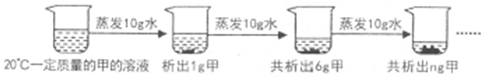
| A. | 蒸发前原溶液是饱和溶液 | B. | 甲的溶解度随温度的升高而减小 | ||
| C. | n的数值是11 | D. | 20℃时甲的溶解度是6g |
| A. | 紫色石蕊试液 | B. | 铁粉 | C. | 氯化钠溶液 | D. | pH试纸 |
| A. | 滤液可能是无色 | B. | 滤液中一定有 ZnCl2 和 FeCl2 | ||
| C. | 滤渣中的物质可能有3种 | D. | 滤渣中加稀盐酸一定有气泡产生 |
 镁是一种活泼金属,除了能与氧气反应,还能与氮气、二氧化碳等反应.为测定镁铝合金(不 含其它元素)中镁的质量分数,称量 ag 镁铝合金粉末,放在如图所示装置的惰性电热板上,通 电使其充分灼烧.下列关于该实验的说法错误的是( )
镁是一种活泼金属,除了能与氧气反应,还能与氮气、二氧化碳等反应.为测定镁铝合金(不 含其它元素)中镁的质量分数,称量 ag 镁铝合金粉末,放在如图所示装置的惰性电热板上,通 电使其充分灼烧.下列关于该实验的说法错误的是( )| A. | 氧气要保证充足 | |
| B. | 实验结束后一定要再次称量剩余固体质量 | |
| C. | 用空气代替氧气对实验没有影响 | |
| D. | 灼烧后的固体为氧化镁和氧化铝的混合物,质量大于 ag |

 如图是a、b、c三种物质的溶解度曲线,请回答下列问题
如图是a、b、c三种物质的溶解度曲线,请回答下列问题