题目内容
9.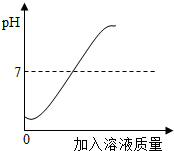 酸与碱作用生成盐和水的反应,叫中和反应.在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:
酸与碱作用生成盐和水的反应,叫中和反应.在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:(1)要得到此变化曲线,所进行的操作是②(填序号).
①将稀盐酸滴加到氢氧化钠溶液中
②将氢氧化钠溶液滴加到稀盐酸中
(2)该反应的化学方程式NaOH+HCl=NaCl+H2O.
(3)当溶液的PH=7时,溶液中Na+与Cl-的个数比为1:1.
分析 根据图象中pH值的变化是从小于7逐渐的增大到大于7,可以分析确定操作的过程,根据反应物盐酸和氢氧化钠中和生成水和氯化钠的过程,依照书写规则书写化学反应方程式,当溶液的pH=7时,盐酸和氢氧化钠恰好完全反应,溶液中Na+与Cl-的个数比为1:1进行分析.
解答 解:(1)由图象可知,pH值是从小于7 逐渐的增大到7然后在大于7,可知原溶液是酸性的,然后不断的加碱,使pH升高,故选:②;
(2)氢氧化钠和盐酸发生中和反应生成氯化钠和水的过程,化学方程式为:NaOH+HCl=NaCl+H2O;
(3)当溶液的pH=7时,盐酸和氢氧化钠恰好完全反应,溶液中Na+与Cl-的个数比为:1:1.
故答案为:(1)②;
(2)NaOH+HCl=NaCl+H2O;
(3)1:1.
点评 本题主要考查了从图象的角度对中和反应的正确理解,要学会这种数形结合的思想.

练习册系列答案
相关题目
17.下列说法中正确的是( )
| A. | 二氧化碳能使干燥的紫色石蕊试纸变红 | |
| B. | 加入二氧化锰能使氯酸钾分解出更多氧气 | |
| C. | 铁制容器盛装硫酸铜溶液时会被腐蚀 | |
| D. | 含有碳酸氢钠的药物可中和胃液里过多的胃酸 |
14.下列各组物质中,能在水溶液中大量共存的一组是( )
| A. | NaCl NaOH KNO3 | B. | Ba(NO3)2 KNO3 H2SO4 | ||
| C. | Ca(OH)2 HCl KCl | D. | Na2CO3 CaCl2 HNO3 |
1.下列化学方程式的书写不正确的是( )
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | CH4+O2═CO2+H2O | ||
| C. | 4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3 | D. | CO2+Ca(OH)2═CaCO3↓+H2O |
18.依据图分析,下列说法正确的是( )
| A. |  用一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系 用一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系 | |
| B. |  向等质量的金属镁和锌中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系 向等质量的金属镁和锌中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系 | |
| C. |  B点显示此时某绿色植物没有进行光合作用和呼吸作用 B点显示此时某绿色植物没有进行光合作用和呼吸作用 | |
| D. |  曲线表示某人的呼吸频率是20次/分钟 曲线表示某人的呼吸频率是20次/分钟 |
 如图是两套实验室常用的气体制取装置.请回答:
如图是两套实验室常用的气体制取装置.请回答: