题目内容
8.化学物质及其变化与生活密切相关.①健康人的体液PH必须维持在一定的范围内.如果体液pH超越正常范围,就会导致某些疾病的产生.胃液的pH<7(选填“>”,“<”或“=”).
人体内的二氧化碳排出不畅时,会导致血液pH降低(选填“升高”或“降低”).
②自来水中含有少量的Ca(HCO3)2和MgSO4等可溶性盐.
烧开水的壶中会出现水垢的原因之一是其中的Ca(HCO3)2发生了分解反应,生成了难溶的CaCO3.请写出Ca(HCO3)2受热分解的化学方程式:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O.
实验室若用自来水配制Ba(OH)2溶液,可能出现的现象是:溶液浑浊;造成这种现象的原因是(请用其中一个反应的化学方程式表示)MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓或Ca(HCO3)2+Ba(OH)2=CaCO3↓+BaCO3↓+2H2O;.
分析 (1)利用胃液中含有盐酸的知识解决,酸性越强PH越小.
(2)利用信息结合方程式的书写要求解决,氢氧化钡可能与水中的少量硫酸镁或碳酸氢钙反应生成硫酸钡的沉淀.
解答 解:(1)胃液中含有少量的盐酸其PH会小于7,二氧化碳与水反应会生成少量的碳酸,使血液中的酸性增强PH下降.
故答案为:<;降低.
(2)碳酸氢钙受热会生成碳酸钙水与二氧化碳,氢氧化钡与自来水中的硫酸镁或碳酸氢钙反应会生成硫酸钡或碳酸钡的沉淀.
故答案为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O;溶液浑浊;MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓或Ca(HCO3)2+Ba(OH)2=CaCO3↓+BaCO3↓+2H2O;
点评 此题是一道生活实际的考查题,解题的关键是对化学与生活实际的联系的掌握,属基础性知识考查题.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
18.列反应,属于分解反应的是( )
| A. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | |
| B. | 碳酸钙$\stackrel{点燃}{→}$氧化钙+二氧化碳 | |
| C. | 乙醇+氧气$\stackrel{点燃}{→}$二氧化碳+水 | |
| D. | 氯化铁+氢氧化钠=氢氧化铁+氯化钠 |
19.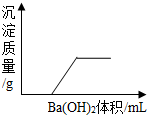 有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )
有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )
 有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )
有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )| A. | 硝酸、硝酸铁 | B. | 硝酸、硫酸铁 | C. | 盐酸、氯化铁 | D. | 盐酸、硝酸铁 |
3.下列各组物质不能发生复分解反应的是( )
| A. | CaCO3+HCl | B. | K NO3+BaCl2 | C. | BaCl2+H2SO4 | D. | AgNO3+HCl |
20.对于有单质和化合物生成的反应,有下列几种说法,其中正确的是( )
| A. | 一定是置换反应 | B. | 不可能是化合反应 | ||
| C. | 一定是化合反应 | D. | 一定是分解反应 |
17.某些金属工艺品的外观有银白色的金属光泽,有的同学认为它可能和铁一样,有磁性.有的同学认为它可能和银一样,无磁性.他们的争论属于科学探究中的( )
| A. | 假设 | B. | 实验 | C. | 设计方案 | D. | 得出结论 |
18.下列实验操作能达到预期目的是( )
| A. | 用闻气味的方法鉴别CO和CO2气体 | B. | 用NaOH溶液除去CO2中的HCl气体 | ||
| C. | 用托盘天平称取3.27 gNaCl固体 | D. | 用排水法收集氧气 |
