题目内容
15.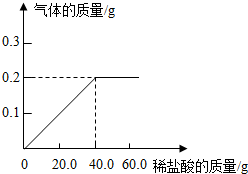 黄铜(铜锌合金)是重要的金属材料,常用来制造机械零件、仪表和日用品.为测定某黄铜材料中锌的含量,化学研究小组进行了实验:称取15.0g此黄铜材料,向其中逐渐加入稀盐酸,测定产生气体的质量和加入稀盐酸的质量,并根据实验情况绘制了产生气体质量与加入稀盐酸质量的关系图.
黄铜(铜锌合金)是重要的金属材料,常用来制造机械零件、仪表和日用品.为测定某黄铜材料中锌的含量,化学研究小组进行了实验:称取15.0g此黄铜材料,向其中逐渐加入稀盐酸,测定产生气体的质量和加入稀盐酸的质量,并根据实验情况绘制了产生气体质量与加入稀盐酸质量的关系图.请你仔细分析此关系图,并进行计算:
(1)15.0g黄铜材料中含锌6.5g.
(2)稀盐酸中溶质的质量分数(写出计算过程),计算结果精确到0.1%).
分析 (1)根据锌会与稀盐酸反应生成氯化锌和氢气,结合题中的数据进行计算;
(2)根据生成的氢气和参加反应的盐酸的质量进行计算.
解答 解:设参加反应的锌的质量为x,参加反应的纯净的盐酸为y,
Zn+2HCl=ZnCl2+H2↑
65 73 2
x y 0.2g
$\frac{65}{x}$=$\frac{73}{y}$=$\frac{2}{0.2g}$
x=6.5g
y=7.3g
所以稀盐酸中溶质的质量分数为:$\frac{7.3g}{40g}$×100%≈18.3%.
故答案为:(1)6.5;
(2)18.3%.
点评 有关反应后所得溶液的计算是初中化学的一个重点,需要认真分析反应原理.

练习册系列答案
相关题目
5.除去下列物质中的少量杂质,所选用的试剂,操作方法及反应类型都正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 | 反应类型 |
| A | MnO2 | KCl | 适量水 | 溶解、过滤、蒸发结晶 | / |
| B | CO2 | CO | 足量氧气 | 点燃 | 化合反应 |
| C | CaO | CaCO3 | 稀盐酸 | 过滤 | 复分解反应 |
| D | NaOH溶液 | Ca(OH)2 | 适量Na2CO3溶液 | 过滤 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
10.下表是某食品包装说明中的部分内容.请你从配料中选择物质填空.
(1)富含蛋白质的是鲜鸡蛋.
(2)精炼植物油是人体重要的供能物质,并能在人体内储存起来,成为维持生命活动的备用能源.
| 品名 | ××× |
| 配料 | 鲜鸡蛋、精面粉、精炼植物油、白砂糖、食盐、柠檬汁、食品添加剂 |
| 保质期 | 240天 |
| 生产日期:见封口处 | |
(2)精炼植物油是人体重要的供能物质,并能在人体内储存起来,成为维持生命活动的备用能源.
20.水是生产生活中不可缺少的物质.下列关于水的说法中正确的是( )
| A. | 明矾溶液可以区分硬水和软水 | |
| B. | 在自来水厂净化水的过程中,发生的变化都是物理变化 | |
| C. | 水与过氧化氢的组成元素相同,均可用于制备氧气 | |
| D. | 为了节约用水,可以用工业废水直接浇灌农田 |
12.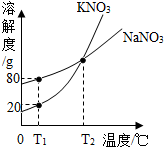 如图表示的是KNO3和NaNO3的溶解度曲线,下列说法正确的是( )
如图表示的是KNO3和NaNO3的溶解度曲线,下列说法正确的是( )
 如图表示的是KNO3和NaNO3的溶解度曲线,下列说法正确的是( )
如图表示的是KNO3和NaNO3的溶解度曲线,下列说法正确的是( )| A. | T2℃时,KNO3溶液的浓度一定等于NaNO3溶液的浓度 | |
| B. | T1℃时,在50g水里加入15g KNO3固体,充分溶解,可得到65g溶液 | |
| C. | T1℃时,往180g NaNO3饱和溶液中加入620g水可配成质量分数为10%的NaNO3溶液 | |
| D. | 若KNO3中混有少量NaNO3,可用蒸发溶剂的方法提纯 |
13. 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A. | t1℃时,甲、乙两种物质的饱和溶液中溶质的质量相等 | |
| B. | 将甲、乙的饱和溶液从t2℃降到t1℃,两者均有晶体析出 | |
| C. | 将甲的溶液从t1℃升到t2℃,其溶质的质量分数一定增大 | |
| D. | 当温度高于t1℃而低于t2℃时,乙的溶解度比甲的溶解度小 |
 低钠盐是一种健康食盐,以普通钠盐为基础添加一定量氯化钠(氯化钠70%左右,氯化钾30%左右),有助于人体钠、钾平衡,降低高血压、心血管疾病的患病风险.另外,由于食盐中导致咸味的是氯离子,因此,低钠盐能较好实现减钠补钾不减咸味的目的.
低钠盐是一种健康食盐,以普通钠盐为基础添加一定量氯化钠(氯化钠70%左右,氯化钾30%左右),有助于人体钠、钾平衡,降低高血压、心血管疾病的患病风险.另外,由于食盐中导致咸味的是氯离子,因此,低钠盐能较好实现减钠补钾不减咸味的目的.