题目内容
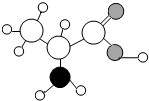 (1)
(1) ”表示氮原子;“
”表示氮原子;“ ”表示碳原子;“
”表示碳原子;“ ”表示氧原子;“
”表示氧原子;“ ”表示氢原子,“-”表示原子之间相互连接.)则α-丙氨酸中含有
”表示氢原子,“-”表示原子之间相互连接.)则α-丙氨酸中含有(2)质量相等的铁、镁、铝三种金属分别与足量的稀硫酸反应,生成氢气的质量比为:
考点:化学式的书写及意义,金属的化学性质,相对分子质量的概念及其计算,元素质量比的计算,根据化学反应方程式的计算
专题:化学用语和质量守恒定律,金属与金属材料
分析:(1)根据α-丙氨酸的分子结构图,确定其化学式,进而由α-丙氨酸化学式的含义、化合物中各元素质量比=各原子的相对原子质量×原子个数之比、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)利用四种物质与酸的反应的化学方程式分析判断,进而确定其质量比.
(2)利用四种物质与酸的反应的化学方程式分析判断,进而确定其质量比.
解答:解:(1)由α-丙氨酸的分子结构图可知,一个α-丙氨酸分子中含有3个碳原子、7个氢原子、2个氧原子、1个氮原子,其化学式为:C3H7O2N;则α-丙氨酸中含有碳、氢、氧、氮四种元素;其中碳、氧两种元素质量比为(12×3):(16×2)=9:8;其相对分子质量为12×3+1×7+16×2+14×1=89.
(2)设三种金属的质量均为x,铁、镁、铝与足量的硫酸反应生成氢气的质量分别为a、b、c
则有:
Fe+H2SO4=FeSO4+H2↑
56 2
x a
=
a=
Mg+H2SO4=MgSO4+H2↑
24 2
x b
=
b=
2Al+3H2SO4=Al2(SO4)3+3H2↑
54 6
x c
=
c=
质量相等的铁、镁、铝三种金属分别与足量的稀硫酸反应,生成氢气的质量比为:
:
:
=
:
:
.
故答案为:(1)4;9:8;89;(2)
:
:
.
(2)设三种金属的质量均为x,铁、镁、铝与足量的硫酸反应生成氢气的质量分别为a、b、c
则有:
Fe+H2SO4=FeSO4+H2↑
56 2
x a
| 56 |
| 2 |
| x |
| a |
| x |
| 28 |
Mg+H2SO4=MgSO4+H2↑
24 2
x b
| 24 |
| 2 |
| x |
| b |
| x |
| 12 |
2Al+3H2SO4=Al2(SO4)3+3H2↑
54 6
x c
| 54 |
| 6 |
| x |
| c |
| x |
| 9 |
质量相等的铁、镁、铝三种金属分别与足量的稀硫酸反应,生成氢气的质量比为:
| x |
| 28 |
| x |
| 12 |
| x |
| 9 |
| 1 |
| 28 |
| 1 |
| 12 |
| 1 |
| 9 |
故答案为:(1)4;9:8;89;(2)
| 1 |
| 28 |
| 1 |
| 12 |
| 1 |
| 9 |
点评:本题难度不大,考查同学们结合分子结构图、灵活运用化学式的有关计算以及化学方程式的计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
下列不能将稀盐酸和水鉴别开来的是( )
| A、CuO |
| B、Na2CO3 |
| C、酚酞 |
| D、石蕊 |
有关下列叙述中,错误的是( )
| A、油污可以被洗涤剂通过乳化作用除去 |
| B、将熟石灰掺入燃煤中可以减少对空气污染 |
| C、碳铵应低温贮存,使用时不能与草木灰(主要成分是碳酸钾)混合施用 |
| D、在图书档案、贵重设备、精密仪器等发生火灾时,可用泡沫灭火器扑灭 |