题目内容
10.有一包固体粉末,可能含有碳酸钙、硫酸铜、硝酸钾、硫酸钠、氯化钡中的一种或几种.为确定其组成,进行如下实验:(填写物质的名称)(1)取该固体粉末少量加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液;
(2)过滤,在白色沉淀中加入足量稀硝酸,白色沉淀不溶解.根据以上实验可推断原固体粉末中一定有的物质是硫酸钠和氯化钡;一定没有的物质是硫酸铜、碳酸钙;不能确定的物质是硝酸钾;
(3)为确定这包固体粉末的组成,小华取原固体粉末8.00g加足量水充分溶解后,其粉末中的成分恰好完全反应,过滤,将沉淀洗涤、干燥.称得其质量为4.66g.通过计算后,确定这包固体粉末的组成是硫酸钠、氯化钡、硝酸钾.
分析 根据碳酸钙难溶于水会溶于酸,硫酸铜在溶液中显蓝色,硫酸钡沉淀不溶于水也不溶于酸进行分析.
解答 解:取该固体粉末少量加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液,可以确定没有硫酸铜,白色沉淀中加入足量的稀硝酸,白色沉淀不溶解,说明白色沉淀不是碳酸钙,是硫酸钡,说明混合物中没有碳酸钙,有氯化钡和硫酸钠,硝酸钾对上面的实验现象不会产生影响,所以无法确定硝酸钾的存在,故答案为:硫酸钠和氯化钡;硫酸铜、碳酸钙;硝酸钾;
设生成4.66克的沉淀需要氯化钡x,硫酸钠y,
BaCl2+Na2SO4=2NaCl+BaSO4↓
208 142 233
x y 4.66g
$\frac{208}{x}=\frac{142}{y}=\frac{233}{4.66g}$
x=4.16g,y=2.84g
故氯化钡和硫酸钠的质量之和为7g,小于8g,所以存在硝酸钾.
故答案为:硫酸钠、氯化钡、硝酸钾.
点评 在解此类题时,首先要弄清楚混合物中各种物质的性质,然后根据题中的现象进行逐一的对照分析.在根据化学方程式计算时,书写方程式,列出比例式是关键.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
20.物质是变化的,我们生活在多姿多彩的物质世界里.下列变化中有新物质生成的是( )
| A. | 灯泡通电发光 | B. | 金刚石加工成钻石 | ||
| C. | 干冰升华 | D. | 葡萄酿成葡萄酒 |
18.下表中,有关量的变化图象与其对应叙述相符的是( )
| A. | 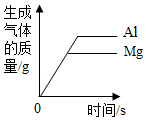 等质量的铝和镁分别与足量的等溶质质量分数的稀硫酸充分反应 等质量的铝和镁分别与足量的等溶质质量分数的稀硫酸充分反应 | |
| B. | 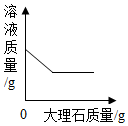 向一定质量的稀盐酸中加入大理石 向一定质量的稀盐酸中加入大理石 | |
| C. | 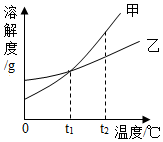 将甲、乙两种物质的饱和溶液分别从t2℃降温至t1℃时,析出晶体的质量甲不一定大于乙 将甲、乙两种物质的饱和溶液分别从t2℃降温至t1℃时,析出晶体的质量甲不一定大于乙 | |
| D. | 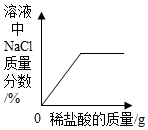 向一定质量的氢氧化钠溶液中加入稀盐酸 向一定质量的氢氧化钠溶液中加入稀盐酸 |
2.向盛有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下.请分析并回答下列问题:
(1)当加入氢氧化钠溶液的体积为10mL时,稀盐酸和氢氧化钠溶液恰好完全反应;
(2)请你写出此过程中发生的化学反应方程式NaOH+HCl=NaCl+H2O.
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?NaCl和HCl(或氯化钠和氯化氢).
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
(2)请你写出此过程中发生的化学反应方程式NaOH+HCl=NaCl+H2O.
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?NaCl和HCl(或氯化钠和氯化氢).
19.在元旦晚会上小明表演了-个魔术:他拿出一把装满“水”的“宝壶”,分别向编号为ABCDEF六只烧杯(装有少量不同试剂)中倒“水”,结果A杯无色透明,B杯看似红墨水,C杯看似蓝墨水,D杯看似牛奶,E杯看似红褐色涂料,F杯看似蓝色果冻.则宝壶中的“水”可能是( )
| A. | NaOH溶液 | B. | HCl溶液 | C. | CuSO4溶液 | D. | FeCl3溶液 |
