题目内容
7.某学校的课外活动小组要测定某块盐碱地中的NaCl、Na2SO4、Na2CO3的含量,为盐碱地的改造提供依据.他们进行了合理采样、晾干、粉碎、称量,加蒸馏水充分搅拌后过滤,得到滤液,并对所取滤液进行以下实验: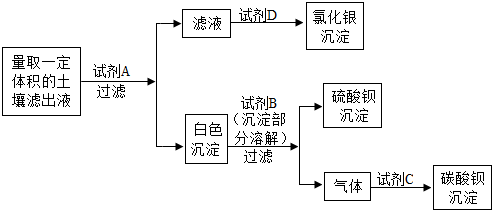
实验过程中所加试剂均是足量的,得到的所有沉淀中的阴离子都来自原土壤滤出液中.最后,称量实验中得到的各种沉淀质量,计算得出盐碱地中上述三种盐的含量.
请回答下列问题:
(1)上述实验中试剂A的化学式是Ba(NO3)2,试剂B的化学式是HNO3或HCl,气体和试剂C反应的化学方程式是CO2+Ba(OH)2═BaCO3↓+H2O.
(2)若上述实验中试剂A为氯化钡溶液,则按上述实验步骤最终测得土壤中NaCl(或氯化钠)的含量偏高.
分析 (1)根据物质的性质分析解答;根据图示,首先加入硝酸钡将氯化钠分离出来;然后再根据碳酸钡可溶于酸,硫酸钡不溶于酸,通过测定硫酸钡的质量进而计算硫酸钠的质量;再通过生成碳酸钡的质量计算所含碳酸钠的质量;
(2)无论测定哪种盐的含量,都要排除干扰;若加入试剂A为氯化钡溶液,则会增加溶液中氯离子的量,使生成的氯化银质量增加,从而造成土壤中氯化钠的含量偏高.
解答 解:(1)氯化钠可以加入硝酸银,通过测定氯化银的质量确定氯化钠的质量;硫酸钠可以加入钡盐,通过生成的硫酸钡确定硫酸钠的质量;根据图示,首先加入硝酸钡将氯化钠分离出来;然后再根据碳酸钡可溶于酸,硫酸钡不溶于酸,通过测定硫酸钡的质量进而计算硫酸钠的质量;再通过生成二氧化碳与氢氧化钡反应生成碳酸钡的质量计算所含碳酸钠的质量;
(2)无论测定哪种盐的含量,都要排除干扰;若加入试剂A为氯化钡溶液,则会增加溶液中氯离子的量,使生成的氯化银质量增加,从而造成土壤中氯化钠的含量偏高;
故答案为:
(1)Ba(NO3)2; HNO3或HCl;CO2+Ba(OH)2═BaCO3↓+H2O;
(3)NaCl(或氯化钠).
点评 本题考查了学生分析、加工信息,并根据所学知识解决问题的能力,在设计实验测定物质含量时,要注意排除干扰.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.喝茶在我国有悠久的历史,“西湖龙井”享有盛名,为保茶叶的品质,要做到防潮和防氧化.为此在茶叶的包装袋内往往放入一小包黑色的还原铁粉作为“双吸剂”,失效后会变成棕黄色物质(氧化铁).请问这一从黑色物质到棕黄色物质的变化过程属于( )
| A. | 化学性质 | B. | 物理性质 | C. | 化学变化 | D. | 物理变化 |
15.以下对某一主题知识进行的归纳,正确的一组是( )
| A. | 健康常识 ①人体缺铁--易患贫血病 ②人体缺锌--易患佝偻病 ③人体缺碘--易患大脖子病 | |
| B. | 安全常识 ①不明洞穴探险--先做灯火实验 ②家中石油气泄漏--立即打开排气扇 ③氢气还原氧化铜--开始时先通氢气再加热 | |
| C. | 事实与解释 ①闻到花香--分子在不停地运动 ②水通电--化学反应中分子可分 ③双氧水能杀菌而水不能--分子结构不同 | |
| D. | 物质分类 ①常见的碱--熟石灰.烧碱.纯碱 ②常见的干燥剂--浓硫酸、生石灰、碱石灰 ③可燃性物质--氢气、氧气、一氧化碳 |
2.下列化学实验操作中,正确的是( )
| A. | 熄灭酒精灯时,用嘴吹灭 | |
| B. | 滴加药品时,胶头滴管应悬在试管口上方 | |
| C. | 稀释浓硫酸时,把水倒入浓硫酸中 | |
| D. | 将实验时多取的药品放回原试剂瓶中 |
19.“好山、好水、好空气”是贵阳引以为傲的金字招牌,下列气体为空气主要成分之一的是( )
| A. | 氧气 | B. | 一氧化碳 | C. | 二氧化氮 | D. | 二氧化硫 |
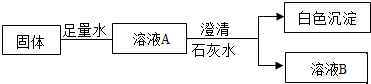
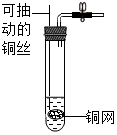
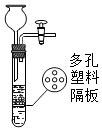
 已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见的金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出.)
已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见的金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出.)