题目内容
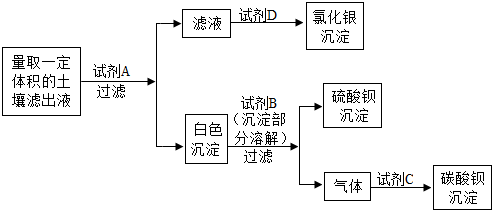
17.有一包固体,可能含有氧化钙、硝酸钾、碳酸钠、碳酸钙中的一种或几种.为探究其组成进行如下实验.①固体中一定含有碳酸钠.
②固体中一定没有氧化钙、碳酸钙.
③写出生成白色沉淀的化学反应方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
分析 碳酸钙不溶于水,氧化钙能和水反应生成氢氧化钙;
碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
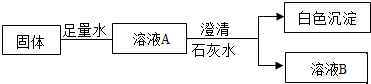
解答 解:向固体中加入足量的水形成溶液,说明固体中不含有碳酸钙;
向溶液A中加入澄清石灰水,石灰水变浑浊,得到白色沉淀,说明固体中含有碳酸钠,如果固体中含有碳酸钠,则固体中不含有氧化钙;
根据实验现象无法确定是否含有硝酸钾;
①固体中一定含有碳酸钠.
故填:碳酸钠.
②固体中一定没有氧化钙、碳酸钙.
故填:氧化钙、碳酸钙.
③碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
7.铝箔常用在食品包装上,因为铝具有良好的( )
| A. | 延展性 | B. | 导电性 | C. | 抗腐蚀性 | D. | 导热性 |
8.氢氟酸(HF)对玻璃有腐蚀作用,可用在玻璃上雕刻各种精美图案,也可用在玻璃仪器上标注刻度文字.氢氟酸与玻璃发生的反应可以表示为:SiO2+4HF═X↑+2H2O,下列说法正确的是( )
| A. | 一定含有硅元素、氟元素 | B. | 可能含有氧元素 | ||
| C. | 可能含有氢元素 | D. | X是一种氧化物 |
5.在探究某种古代金属钱币时,有同学认为他能和铁一样有磁性,提出“先拿磁铁来吸一下”.就“拿磁铁来吸一下”这一过程而言,属于科学探究中的( )
| A. | 假设 | B. | 实验 | C. | 观察 | D. | 做出结论 |
9.水在化学实验中的作用不可忽视,其解释没有体现水的主要作用的是( )
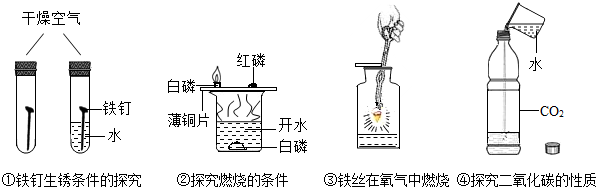

| A. | 实验①中的水:使铁生锈的条件之一 | B. | 实验②中的水:只为了提供能量 | ||
| C. | 实验③中的水:防止集气瓶炸裂 | D. | 实验④中的水:作反应物 |
6.下列现象能表明分子在不停地做无规则运动的是( )
| A. | 无数雨滴从空中落下 | |
| B. | 金属导线导电 | |
| C. | 扫地时,看到空中飞舞的尘埃 | |
| D. | 香水瓶打开后,过一会屋内闻到香味 |