题目内容
4.金属在日常生活和科学研究中有重要应用.(1)铝是比较活泼的金属,为什么铝制品却耐腐蚀?
(2)向一定量的AgNO3和Cu(NO3)2的混合液中加入一定量的锌粉,充分反应后过滤.
①若滤液中只有一种物质,请分析滤渣的成分.
②若滤渣则含有两种固体,请分析滤液的成分.
分析 (1)根据金属铝的化学性质,进行分析解答.
(2)锌的金属活动性比银、铜强,向一定量的AgNO3和Cu(NO3)2的混合液中加入一定量的锌粉,锌先与AgNO3溶液反应生成硝酸锌溶液和银,AgNO3反应完,若还有锌粉,锌才能与Cu(NO3)2溶液反应生成硝酸锌溶液和铜,据此进行分析解答.
解答 解:(1)铝是比较活泼的金属,铝制品却耐腐蚀,是因为铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强.
(2)锌的金属活动性比银、铜强,向一定量的AgNO3和Cu(NO3)2的混合液中加入一定量的锌粉,锌先与AgNO3溶液反应生成硝酸锌溶液和银,AgNO3反应完,若还有锌粉,锌才能与Cu(NO3)2溶液反应生成硝酸锌溶液和铜.
①若滤液中只有一种物质,说明滤液中的溶质是硝酸锌,即硝酸银、硝酸铜均与锌完全反应,可能是恰好完全反应,也可能是锌有剩余,则滤渣的成分是银、铜或银、铜、锌.
②若滤渣则含有两种固体,滤渣中一定含有银和铜,可能是硝酸铜溶液反应了一部分,也可能是完全反应,则滤液的成分可能是硝酸锌、硝酸铜或只有硝酸锌.
故答案为:(1)铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化;
(2)①银、铜或银、铜、锌;②硝酸锌、硝酸铜的混合溶液或只有硝酸锌溶液.
点评 本题难度不是很大,熟练掌握金属的化学性质、综合考虑各种出现的情况是正确解答此类题的关键.

练习册系列答案
相关题目
9.下列我省的一些景点和特色的形成过程中发生了化学变化的是( )
| A. |  华山云海 | B. |  碑石拓片 | ||
| C. |  耀州窑陶瓷 | D. |  户县剪纸 |
14.下列实验操作叙述正确的是( )
| A. | 过滤时,漏斗中液面低于滤纸的边缘 | |
| B. | 加热蒸发过程中,当溶液蒸干时停止加热 | |
| C. | 用量筒量取液体时,仰视或俯视读液体体积 | |
| D. | 倾倒液体时,试剂瓶口紧挨着试管口快速倒入 |
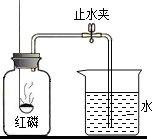 已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示: 晓琳在实验课上发现老师在加热液体时都是使用酒精灯的外焰加热.好奇的她在老师的指导下点燃了酒精灯并进行了探究,实验情景如图所示.
晓琳在实验课上发现老师在加热液体时都是使用酒精灯的外焰加热.好奇的她在老师的指导下点燃了酒精灯并进行了探究,实验情景如图所示.