题目内容
2.某化学兴趣小组学习酸碱中和反应后,对稀盐酸与氢氧化钠溶液混合后的有关问题进行了如下探究.【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
丁同学猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
[实验设计及验证]请将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中, 加入紫色石蕊溶液 | 紫色石蕊溶液变红色 | 丙同学的猜想正确 |
| 取反应后的溶液于试管中, 加入硫酸铜溶液(合理即可) | 有蓝色沉淀生成 | 丁同学的猜想正确 |
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)根据所学化学知识,要验证氢氧化钠溶液与稀盐酸混合后所得溶液中溶质的成分含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?a、c(填序号)
a.pH试纸 b.铜 c.锌粒 d.硝酸银溶液.
分析 【作出猜想】如果氢氧化钠没有完全反应,则溶液的中含有氯化钠和氢氧化钠,由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存,可以据此解答;
【实验设计及验证】盐酸显酸性,能够使石蕊试液变成红色,氢氧化钠溶液可以和氯化铜溶液反应生成蓝色沉淀,可以据此解答该题;
【反思交流】根据实验的结论进行发生反思;
(2)根据盐酸的性质进行分析,但注意氯化钠中也含有氯离子;
解答 解:【作出猜想】如果氢氧化钠没有完全反应,则溶液的中含有氯化钠和氢氧化钠,所以你的猜想为溶质为NaCl和NaOH;由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存,即甲猜想是错误的.
【实验设计及验证】盐酸显酸性,能够使石蕊试液变成红色,则说明丙猜想是正确的;氢氧化钠溶液可以和氯化铜溶液反应生成蓝色沉淀,所以取反应后的溶液于试管中,加入氯化铜溶液,若观察到蓝色沉淀产生,则说明丁的猜想正确;
【实验反思】(1)因为反应可能是完全反应,也可能是其中的一种反应物过量,因此在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量;
(2)因为烧杯内溶液中的溶质含有HCl显酸性,故用pH试纸测定pH应该小于7,但不能和排在氢后面的铜反应,虽然能够和硝酸银反应产生沉淀,但由于其中的氯化钠也能够和硝酸银产生相同的现象,不能选择,故选择ac;
故答案为:【作出猜想】NaCl和NaOH;
由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存;
【实验设计及验证】实验现象:紫色石蕊溶液变红色;
实验操作:硫酸铜溶液(合理即可);
【反思交流】(1)反应物的用量 (2)a、c.
点评 本题考查了酸碱中和反应以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手;检验时要注意氯离子的干扰.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列关于溶液的叙述正确的是( )
| A. | 汽油洗衣服上的油污是利用了乳化作用 | |
| B. | 硝酸铵固体溶于水时仅发生扩散吸热的过程 | |
| C. | 某物质的不饱和溶液变为饱和溶液后溶质质量分数可能不变 | |
| D. | “波尔多液”是无色、透明、均一稳定的混合物 |
13.下列物质呈碱性的是( )
| A. | 食盐水 pH=7 | B. | 炉具清洁剂 pH=12 | ||
| C. | 酱油pH=4 | D. | 柠檬汁pH=3 |
10.下列有关化学家和化学史的叙述中,不正确的是( )
| A. | 法国科学家拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积的$\frac{1}{5}$的结论 | |
| B. | 英国科学家汤姆生提出元素周期律,并发明元素周期表 | |
| C. | 我国古代三大化学工艺为造纸、制火药、烧瓷器 | |
| D. | 我国化学家侯德榜在改进纯碱的生产方面做出了杰出贡献 |
7.工业上镀铜车间的废水中常含有氯化铜和盐酸,化学兴趣小组的学生想测定其中两种成分的含量,以确定其处理方案,于是集取了100g的废水,向其中加入熟石灰进行中和处理,实验过程及处理数据如下.(假设氯化铜溶液为中性)
(1)凌浩同学的实验方案发生的化学方程式是Ca(OH)2+2HCl═CaCl2+2H2O.
(2)月月同学的方案中,与氯化铜反应的熟石灰质量是7.4g.
| 凌浩同学 | 月月同学 | |
| 取废液的质量 | 100g | 100g |
| 加入熟石灰的质量 | 3.7g | 11.1g |
| 加入熟石灰后现象 | 溶液呈蓝色中性,无不溶物 | 溶液呈无色中性,有蓝色沉淀 |
(2)月月同学的方案中,与氯化铜反应的熟石灰质量是7.4g.
12.一定条件下将二氧化碳压缩成干冰,从分子角度解释为( )
| A. | 分子之间有间隙 | B. | 分子可以再分 | ||
| C. | 分子在不断运动 | D. | 分子体积可以变小 |
 水与人类的生活和生产密切相关,请回答下列问题:
水与人类的生活和生产密切相关,请回答下列问题: 如图所示的是几种常见物质的转化关系图,其中A、甲、乙、丙、丁都是化合物,且都含有两种相同的元素.已知甲是有毒的气体,乙是一种酸,丙在一定的条件下可转化为丁(部分反应物、生成物及反应条件已略去).请回答下列问题:
如图所示的是几种常见物质的转化关系图,其中A、甲、乙、丙、丁都是化合物,且都含有两种相同的元素.已知甲是有毒的气体,乙是一种酸,丙在一定的条件下可转化为丁(部分反应物、生成物及反应条件已略去).请回答下列问题: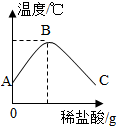 将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示.
将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示.