题目内容
把一定量的锌粒浸入硫酸铜溶液中完全反应,若需要得到16g的金属铜,将耗用金属锌多少克?(保留小数后2位)
解:设锌的质量为x
Zn+CuSO4=ZnSO4+Cu
65 64
x 16g
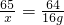 x=16.25g 答:耗用金属锌的质量为:16.25g.
x=16.25g 答:耗用金属锌的质量为:16.25g.
故答案为:16.25g.
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,锌与硫酸铜溶液反应生成硫酸锌和铜,根据铜的质量可以求出锌的质量.
点评:本考点是有关化学方程式的计算题,属于文字叙述型计算题.本题是已知生成物的质量求反应物的质量,从不同的方面考查了学生的分析能力和计算能力.化学方程式要写正确,始终不要忘记质量守恒定律,同学们要认真把握.
Zn+CuSO4=ZnSO4+Cu
65 64
x 16g
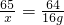 x=16.25g 答:耗用金属锌的质量为:16.25g.
x=16.25g 答:耗用金属锌的质量为:16.25g.故答案为:16.25g.
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,锌与硫酸铜溶液反应生成硫酸锌和铜,根据铜的质量可以求出锌的质量.
点评:本考点是有关化学方程式的计算题,属于文字叙述型计算题.本题是已知生成物的质量求反应物的质量,从不同的方面考查了学生的分析能力和计算能力.化学方程式要写正确,始终不要忘记质量守恒定律,同学们要认真把握.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目