题目内容
15.如表为元素周期表中某一周期元素的原子结构示意图.
请回答下列问题:
(1)表中具有相对稳定结构的元素是氩(填名称).
(2)在化学反应中,铝原子易失去(填“得到”或“失去”)电子形成铝离子.
(3)钠元素与氯元素形成的化合物化学式为NaCl.
(4)上述元素在周期表中处于同一周期的原因是电子层数相同.
(5)日本核泄漏,仍在继续影响周边地区安全.人工放射性核素碘-131,该碘原子(I)的结构示意图如图所示.下列原子对应的元素与碘元素化学性质相似的C(填字母).

分析 (1)根据最外层电子数决定元素的化学性质来分析;
(2)根据铝原子的最外层电子数来分析;
(3)根据化学式的写法来分析;
(4)根据元素周期数与电子层数的关系进行分析解答.
(5)由最外层电子数决定元素的化学性质,判断与碘原子最外层电子数相等的原子.
解答 解:(1)最外层电子数为8的原子是稳定结构,观察各原子结构示意图可知氩原子最外层有8个电子,处于稳定结构;故填:氩;
(2)根据铝原子的结构示意图可知,其最外层有3个电子,在化学反应中易失去3个电子而带3个单位的正电荷.故填:失去;
(3)由元素周期表的信息可知,氯元素的原子序数为17,钠元素的相对原子质量为23;氯是17号元素,原子核内有17个质子,核外有17个电子,核外有3个电子层,最外层有7个电子,在化学反应中易得到1个电子,而显-1价,钠原子最外层有一个电子,易失去最外层的一个电子而显+1价,故填:NaCl.
(4)由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.故答案为:电子层数相同.
(5)C原子的最外层电子数与碘原子最外层电子数相同,均为7,因此C原子的所对应的元素的化学性质与碘元素化学性质相似;故填;C.
点评 本题难度不大,是常考的题型,掌握同一周期的各原子结构示意图的特点、化学式的书写等是正确解答此类题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
5.黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
按要求回答下列问题:
(1)(4分)根据实验数据分析,表中m的数值为0.6,n的数值应该为1.0;
(2)(6分)列式计算该黄铜样品中金属铜的质量分数.(要求写出计算过程)
按要求回答下列问题:
(1)(4分)根据实验数据分析,表中m的数值为0.6,n的数值应该为1.0;
(2)(6分)列式计算该黄铜样品中金属铜的质量分数.(要求写出计算过程)
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量(g) | 0.3 | m | 0.9 | 1.0 | n |
6.推理是学习化学的一种重要方法.下列的推理正确的是( )
| A. | 酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应 | |
| B. | 向某溶液中滴加无色酚酞试液,酚酞试液不变色,说明该溶液一定不显碱性 | |
| C. | 酸和碱的溶液能与指示剂反应,所以所有的酸和碱都能使指示剂变色 | |
| D. | 化合物含有不同种元素,所以含有不同种元素的物质一定是化合物 |
3.下列变化属于物理变化的是( )
| A. | 电灯泡通电后发光 | |
| B. | 用葡萄酿酒 | |
| C. | 敞口放置于空气中的石灰水表面出现白膜 | |
| D. | 森林中发生火灾 |
4.人体健康离不开化学.下列叙述不正确的是( )
| A. | 肉类和豆类中富含锌、铁等微量元素 | |
| B. | 青少年每天只需摄入60g-70g的蛋白质 | |
| C. | 纤维素、淀粉都属于糖类.都含有碳、氢、氧元素 | |
| D. | 大量出汗后可以饮用含有无机盐的运动饮料 |
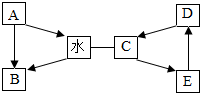 A-E是初中化学常见的物质.A和水具有相同的组成,D是大理石的主要成分,C、D、E 三种物质含有同种金属元素,A、C均属于氧化物,E是碱.图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答:
A-E是初中化学常见的物质.A和水具有相同的组成,D是大理石的主要成分,C、D、E 三种物质含有同种金属元素,A、C均属于氧化物,E是碱.图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答: