题目内容
欲测定某锌-铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= 克;
(2)计算该合金样品中铜的质量分数.
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 20 | 20 | 20 |
| 生成气体质量/g | 0.08 | m | 0.04 |
(1)第二次实验时生成气体质量m=
(2)计算该合金样品中铜的质量分数.
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)分析题中三次数据可以知道,第三次加入稀硫酸后仍然生成气体,所以可以判断第二次生成气体的质量为0.08g,可以据此解答;
(2)根据生成气体的质量结合反应的化学方程式可以计算出锌的质量,然后求出铜的质量分数即可.
(2)根据生成气体的质量结合反应的化学方程式可以计算出锌的质量,然后求出铜的质量分数即可.
解答:解:(1)分析题中三次数据可以知道,第三次加入稀硫酸后仍然生成气体,所以可以判断第二次生成气体的质量为0.08g;
(2)由题意可以知道10g合金与酸反应生成气体的质量为:0.08g+0.08g+0.04g=0.2g
设锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
=
解得:x=6.5g
该合金样品中铜的质量分数为:
×100%=35%
答:该合金样品中铜的质量分数为35%.
(2)由题意可以知道10g合金与酸反应生成气体的质量为:0.08g+0.08g+0.04g=0.2g
设锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| x |
| 2 |
| 0.2g |
解得:x=6.5g
该合金样品中铜的质量分数为:
| 10g-6.5g |
| 10g |
答:该合金样品中铜的质量分数为35%.
点评:本考点考查了表格型计算题,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确.本考点主要出现在计算题中.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
向氧化铜和锌粉的混合物中加入一定量的稀硫酸,反应停止后过滤,再向滤液中插入铁片,铁片无变化,以下判断正确的是( )
| A、滤液中一定含有铜和锌 |
| B、滤液中一定含有Zn2+ |
| C、滤液中一定含有H+ |
| D、滤液中一定含有Cu2+ |
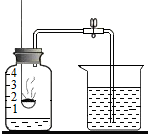 使用红磷燃烧的方法测定空气中氧气的含量:
使用红磷燃烧的方法测定空气中氧气的含量:
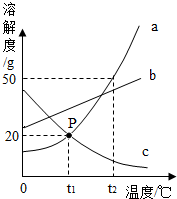 根据如图的溶解度曲线图回答:
根据如图的溶解度曲线图回答: