题目内容
如图是教材中测定空气里氧气含量的实验装置.小华按要求完成了该实验并进一步进行了探究活动.请你帮助小华回答下列问题.(1)该实验中红磷需稍过量,目的是______.
(2)红磷燃烧时产生大量的白烟,写出该反应的化学方程式:______ 2P2O5

【答案】分析:(1)根据实验目的分析红磷过量原因
(2)根据方程式书写原则书写方程式,根据反应类型定义判断反应类型
(3)根据实验现象分析推测氮气的性质
(4)根据实验操作注意事项分析小于五分之一的原因.
解答:解:(1)该实验是测定空气中氧气含量的实验,因此要将氧气全部耗尽,故红磷需稍过.
(2)红磷燃烧生成五氧化二磷,该反应的化学方程式:4P+5O2 2P2O5;该反应反应物是两种,生成物是一种,是化合反应.
2P2O5;该反应反应物是两种,生成物是一种,是化合反应.
(3)水进入约五分之一,由此可知氮气难溶于水,红磷燃烧一会熄灭,集气瓶中剩余约五分之四体积的气体不支持燃烧,不燃烧,因此氮气不燃烧也不支持燃烧.
(4)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.都会使进入的水少于五分之一.
故答案为:(1)为了彻底消耗集气瓶内的氧气(或为了使集气瓶内的氧气充分发生反应)
(2)4P+5O2 2P2O5化合反应 (3)①氮气难溶于水 ②氮气不燃烧,也不支持燃烧 (4)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.(答案合理即可)
2P2O5化合反应 (3)①氮气难溶于水 ②氮气不燃烧,也不支持燃烧 (4)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.(答案合理即可)
点评:本题考查空气中氧气含量测定实验中的基本知识,要明确实验操作步骤及注意事项.
(2)根据方程式书写原则书写方程式,根据反应类型定义判断反应类型
(3)根据实验现象分析推测氮气的性质
(4)根据实验操作注意事项分析小于五分之一的原因.
解答:解:(1)该实验是测定空气中氧气含量的实验,因此要将氧气全部耗尽,故红磷需稍过.
(2)红磷燃烧生成五氧化二磷,该反应的化学方程式:4P+5O2
 2P2O5;该反应反应物是两种,生成物是一种,是化合反应.
2P2O5;该反应反应物是两种,生成物是一种,是化合反应.(3)水进入约五分之一,由此可知氮气难溶于水,红磷燃烧一会熄灭,集气瓶中剩余约五分之四体积的气体不支持燃烧,不燃烧,因此氮气不燃烧也不支持燃烧.
(4)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.都会使进入的水少于五分之一.
故答案为:(1)为了彻底消耗集气瓶内的氧气(或为了使集气瓶内的氧气充分发生反应)
(2)4P+5O2
 2P2O5化合反应 (3)①氮气难溶于水 ②氮气不燃烧,也不支持燃烧 (4)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.(答案合理即可)
2P2O5化合反应 (3)①氮气难溶于水 ②氮气不燃烧,也不支持燃烧 (4)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.(答案合理即可)点评:本题考查空气中氧气含量测定实验中的基本知识,要明确实验操作步骤及注意事项.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
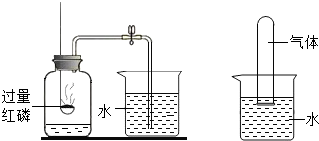 空气主要是由氮气和氧气组成的混合物,请你参与研究性小组有关空气成分测定和性质的实验探究.
空气主要是由氮气和氧气组成的混合物,请你参与研究性小组有关空气成分测定和性质的实验探究.(1)下图是教材中测定空气里氧气含量的实验装置.
填写下表:
| 实验现象 | 结论或解释 |
| 红磷在集气瓶中燃烧 | 反应的化学方程式为: |
| 水倒流入集气瓶中,体积 约占集气瓶体积的1/5 |
结论: |
A.装置漏气 B.红磷过量
C.温度太高 D.氮气溶解
该小组同学根据空气中氧气含量测定的实验,一致认为:氮气不能支持红磷燃烧.你认为该结论是否正确:
(2)该小组的同学对集气瓶中氮气的性质作了进一步的探究.
物理性质探究:
甲同学在实验探究中设计了如右图所示的实验装置.则该同学设计的目的是为了探究氮气的
化学性质探究:
乙同学将点燃的镁条迅速伸入集气瓶中,结果发现镁条继续燃烧,并产生黄色固体.据此,你能得出什么结论:
丙同学用天平称取2.4g表面处理过的镁条,在一个完全封闭且充满足量空气的容器中完全燃烧,产物冷却后再称量,发现固体质量小于4.0g.原因是:
 如图是教材中测定空气里氧气含量的实验装置.小华按要求完成了该实验并进一步进行了探究活动.请你帮助小华回答下列问题.
如图是教材中测定空气里氧气含量的实验装置.小华按要求完成了该实验并进一步进行了探究活动.请你帮助小华回答下列问题. 如图是教材中测定空气里氧气含量的实验装置.小华按要求完成了该实验并进一步进行了探究活动.请你帮助小华回答下列问题.
如图是教材中测定空气里氧气含量的实验装置.小华按要求完成了该实验并进一步进行了探究活动.请你帮助小华回答下列问题. ,还可以推出氮气的有关性质,请写出其中两点:①______;②______.
,还可以推出氮气的有关性质,请写出其中两点:①______;②______.