题目内容
20.某热电厂使用的燃料是含硫较多的煤,附近的居民们怀疑该厂排放出的SO2超标了,于是请兴趣小组帮助测定空气中SO2的含量.【设计实验】兴趣小组的同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品.
(2)向装有空气样品的可乐瓶中少量,多次加入NaOH溶液,每次加入NaOH溶液后都盖紧瓶塞并充分振荡.直至可乐瓶中SO2被完全反应.
(3)加入一定量氧化剂H2O2,使其中的Na2SO3完全转化为Na2SO4.再向可乐瓶中加入过量的BaCl2溶液.
(4)经过过滤、洗涤、烘干,称量固体质量.
(5)根据固体质量计算出SO2的质量,并计算出空气中SO2的含量.
【得出结论】考虑到空气中的各种气体成分,有同学认为求出的SO2的含量偏大,其依据是空气中的二氧化碳参与反应,最终生成碳酸钡沉淀影响计算结果;请提出实验的改进方案:在第(3)步生成的沉淀中滴加稀硝酸直至无气泡产生.同学们通过改进后的方案测出空气中SO2的含量超过了国家标准.
【解决问题】
(1)为了减少SO2的排放,可在含硫煤燃烧时添加生石灰进行固硫,使SO2转化为CaSO3,其中CaSO3中S的化合价为+4.
(2)大气中的SO2会和O2、CO2等一起从叶表皮的气孔(填结构名称)进入叶内,若SO2浓度较高,叶片会出现伤斑,影响植物的正常生长.实验测得甲、乙、丙三种植物在相同浓度SO2的影响下,叶片的平均伤斑面积如表所示,则该热电厂附近,可以选择表中甲(选填“甲”、“乙”或“丙”)植物作为行道树种.
| 被测植物 | 平均伤斑面积(%) |
| 甲 | 13.5 |
| 乙 | 33.4 |
| 丙 | 57.7 |
分析 【得出结论】根据氢氧化钠也能与二氧化碳气体发生反应来分析;
【解决问题】(1)根据化合物中元素化合价的计算方法以及化合物中化合价的代数和为0进行解答;
(2)根据表中信息分析解答.
解答 解:【得出结论】因为空气中含有少量的二氧化碳,当向装有空气样品的可乐瓶中少量,多次加入NaOH溶液,氢氧化钠不但与二氧化硫反应,也与空气中的二氧化碳发生反应,最终生成的沉淀既有硫酸钡也有碳酸钡,影响到了实验结果,造成测量结果偏大,要想准确测定应先除去沉淀中的碳酸钡,可向沉淀中加入稀硝酸直到不再生成气泡为止;故填:空气中的二氧化碳参与反应,最终生成碳酸钡沉淀影响计算结果;在第(3)步生成的沉淀中滴加稀硝酸直至无气泡产生;
【解决问题】(1)在化合物中,钙元素显+2价,氧元素显-2价,设硫元素的化合价为x,则
(+2)+x+(-2)×3=0
x=+4
故填:+4;
(2)大气中的SO2和02、CO2等一起从叶表皮的气孔进入叶内,若S02浓度较高.叶片会出现伤斑,由表中信息可知:甲平均伤斑面积最小,故适合种植甲.
故填:气孔;甲.
点评 本题主要考查了煤的污染,一定要仔细分析题意,提取有用信息,再用所学知识和技能合理解答.综合考查了酸雨的形成、危害,以及化合价的计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质.
【查阅资料】①Na2CO3+CaCl2=CaCO3↓+2NaCl ②2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
③Ca(HCO3)2 易溶于水.
④CaCl2 溶液分别与 NaHCO3、Na2CO3 溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
【进行实验】
【解释与结论】
(1)实验1中,NaHCO3与盐酸反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
(2)实验2中,试剂a为澄清的石灰水.
(3)实验3中,NaHCO3与 CaCl2 反应的化学方程式为:2NaHCO3+CaCl2=CaCO3↓+2NaCl+CO2↑+H2O.
【反思与评价】
(1)实验2中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为Na2CO3;Na2CO3,NaHCO3(写出所有可能).
(2)资料④中,NaHCO3 溶液与 CaCl2溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是CaCl2溶液的溶质质量分数较小,生成的CO2量较少,CO2溶于水,因此没有气泡.
(3)用2种不同的方法鉴别 Na2CO3和NaHCO3固体,实验方案分别为:
①各取少量0.1%的NaHCO3和Na2CO3加入等质量的5%的CaCl2溶液,若无明显现象,则为NaHCO3,若观察到浑浊则为Na2CO3
②各取少量Na2CO3和NaHCO3固体于实验2装置中,分别加热一段时间,若观察到澄清石灰水变浑浊,固体为NaHCO3,若观察到无明显现象,固体为Na2CO3.
【查阅资料】①Na2CO3+CaCl2=CaCO3↓+2NaCl ②2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
| NaHCO3 | Na2CO3 | ||||
| 0.1% | 1% | 5% | 0.1% | ||
CaCl2 | 0.1% | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 1% | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 5% | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
④CaCl2 溶液分别与 NaHCO3、Na2CO3 溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验 1 |  | 向2支试管中分别加入少 量Na2CO3和 NaHCO3溶液,再分别滴加盐酸 | 2支试管中均有气泡产生 |
| 实验 2 | 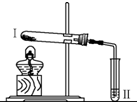 | 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 Na2CO3 或 NaHCO3 固体,分别加热一 段时间 | Na2CO3 受热时Ⅱ中无明 显现象; NaHCO3 受热时Ⅱ中出现 浑浊 |
| 实验 3 |  | 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 5%的 NaHCO3 溶 液,再滴加 5%的 CaCl2 溶 液 | Ⅰ中出现浑浊,有气泡产 生Ⅱ中出现浑浊 |
(1)实验1中,NaHCO3与盐酸反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
(2)实验2中,试剂a为澄清的石灰水.
(3)实验3中,NaHCO3与 CaCl2 反应的化学方程式为:2NaHCO3+CaCl2=CaCO3↓+2NaCl+CO2↑+H2O.
【反思与评价】
(1)实验2中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为Na2CO3;Na2CO3,NaHCO3(写出所有可能).
(2)资料④中,NaHCO3 溶液与 CaCl2溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是CaCl2溶液的溶质质量分数较小,生成的CO2量较少,CO2溶于水,因此没有气泡.
(3)用2种不同的方法鉴别 Na2CO3和NaHCO3固体,实验方案分别为:
①各取少量0.1%的NaHCO3和Na2CO3加入等质量的5%的CaCl2溶液,若无明显现象,则为NaHCO3,若观察到浑浊则为Na2CO3
②各取少量Na2CO3和NaHCO3固体于实验2装置中,分别加热一段时间,若观察到澄清石灰水变浑浊,固体为NaHCO3,若观察到无明显现象,固体为Na2CO3.
11.下列灭火方法及原理均正确的是( )
| A. | 家里油锅着火──锅盖盖灭──隔绝空气 | |
| B. | 废纸篓着火──用水浇灭──降低燃烧物的着火点 | |
| C. | 电器着火──立即用湿棉被盖灭──隔绝空气 | |
| D. | 酒精在桌上燃烧──用水浇灭──降低温度至可燃物着火点以下 |
10.当人被困在火灾现场时,要根据具体情况采取自救措施,下列做法错误的是( )
| A. | 拨打火警电话求救 | B. | 直立身子朝有火光的方向逃生 | ||
| C. | 用湿毛巾或口罩等捂住口鼻 | D. | 蹲下或匍匐前行逃生 |

 已知:白色Fe(OH)2很容易被空气中的氧气氧化为Fe(OH)3,Fe(0H)3为红褐色沉淀,用下面两种方法可以制得白色的Fe(OH)2沉淀.
已知:白色Fe(OH)2很容易被空气中的氧气氧化为Fe(OH)3,Fe(0H)3为红褐色沉淀,用下面两种方法可以制得白色的Fe(OH)2沉淀. 每当电闪雷鸣之时,空气中发生的一种反应为N2+O2═2NO.已知32克氧气和足量的氮气化合成一氧化氮时要吸收150千焦的能量,假设某次闪电的能量为1.50×107千焦,其中有$\frac{1}{1000}$的能量用于这一反应,求:
每当电闪雷鸣之时,空气中发生的一种反应为N2+O2═2NO.已知32克氧气和足量的氮气化合成一氧化氮时要吸收150千焦的能量,假设某次闪电的能量为1.50×107千焦,其中有$\frac{1}{1000}$的能量用于这一反应,求:
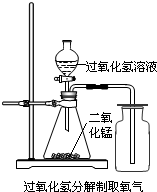 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.