题目内容
某兴趣小组需要10%的氢氧化钠溶液和10%的硫酸溶液,进行中和反应实验.(1)若配制40g上述氢氧化钠溶液,则需要氢氧化钠固体的质量为______g.从下表中选择称量氢氧化钠固体所需要的仪器______.(填序号)
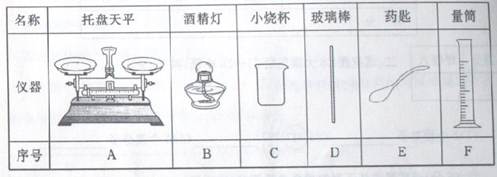
| 名称 | 托盘天平 | 酒精灯 | 小烧杯 | 玻璃棒 | 钥匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | A | B | C | D | E | F |
【答案】分析:(1)利用溶液的溶质质量分数的概念,由溶液质量及溶液质量分数计算溶液中溶质质量;由于所称取的氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,据此选择仪器;
(2)根据氢氧化钠与硫酸反应的化学方程式,确定反应中氢氧化钠与其它物质的质量关系,由氢氧化钠的质量计算反应需要消耗10%的硫酸溶液的质量及反应生成硫酸钠的质量,完成计算.
解答:解:(1)配制40g溶质质量分数为10%的氢氧化钠溶液,需要氢氧化钠的质量=40g×10%=4g;氢氧化钠的强烈腐蚀性要求在称量氢氧化钠时就放在玻璃器皿内,因此称量氢氧化钠时应选用托盘天平、烧杯、药匙三种仪器;
(2)设需10%的硫酸溶液的质量为x,反应生成硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
4g x?10% y
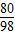 =
=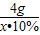 x=49g
x=49g
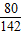 =
=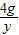 y=7.1g
y=7.1g
反应后所得溶液的溶质质量分数=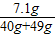 ×100%=7.98%≈8%
×100%=7.98%≈8%
故答案为:(1)4;ACE;(2)49;8%.
点评:根据质量守恒定律,氢氧化钠溶液与稀硫酸反应既无气体也无沉淀产生,因此反应后所得溶液即为氢氧化钠溶液与稀硫酸的质量和.
(2)根据氢氧化钠与硫酸反应的化学方程式,确定反应中氢氧化钠与其它物质的质量关系,由氢氧化钠的质量计算反应需要消耗10%的硫酸溶液的质量及反应生成硫酸钠的质量,完成计算.
解答:解:(1)配制40g溶质质量分数为10%的氢氧化钠溶液,需要氢氧化钠的质量=40g×10%=4g;氢氧化钠的强烈腐蚀性要求在称量氢氧化钠时就放在玻璃器皿内,因此称量氢氧化钠时应选用托盘天平、烧杯、药匙三种仪器;
(2)设需10%的硫酸溶液的质量为x,反应生成硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
4g x?10% y
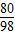 =
=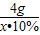 x=49g
x=49g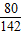 =
=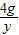 y=7.1g
y=7.1g反应后所得溶液的溶质质量分数=
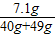 ×100%=7.98%≈8%
×100%=7.98%≈8%故答案为:(1)4;ACE;(2)49;8%.
点评:根据质量守恒定律,氢氧化钠溶液与稀硫酸反应既无气体也无沉淀产生,因此反应后所得溶液即为氢氧化钠溶液与稀硫酸的质量和.

练习册系列答案
相关题目
某兴趣小组需要10%的氢氧化钠溶液和10%的硫酸溶液,进行中和反应实验.
(1)若配制40g上述氢氧化钠溶液,则需要氢氧化钠固体的质量为______g.从下表中选择称量氢氧化钠固体所需要的仪器______.(填序号)
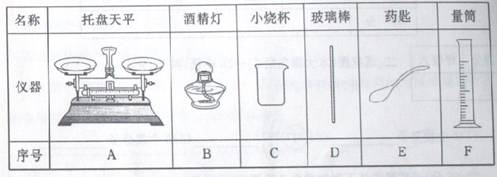
| 名称 | 托盘天平 | 酒精灯 | 小烧杯 | 玻璃棒 | 钥匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | A | B | C | D | E | F |