题目内容
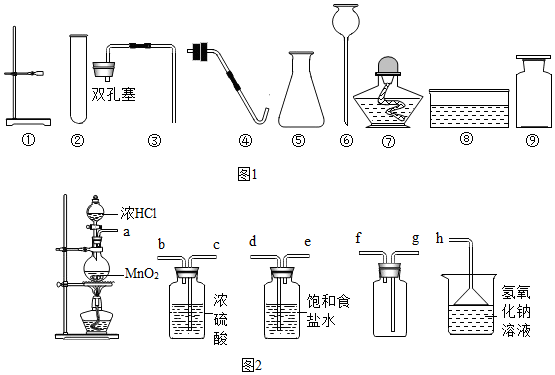
20.实验课上,同学们配制100g质量分数为10%的氢氧化钠溶液做中和反应的实验,图1是配制该溶液的实验操作.
(1)操作①中,需称量氢氧化钠固体的质量是10g.
(2)用图①装置称量氢氧化钠固体,正确的操作是C(填序号).
A、直接放在托盘上称量.
B、在两个托盘上各放一张大小相同的同种纸,将氢氧化钠固体放在左盘纸上称量.
C、先称量一个小烧杯质量,再将氢氧化钠固体放入后称量总质量.
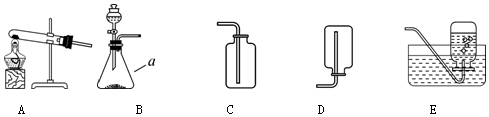
(3)操作②中,玻璃棒的作用是搅拌,加快溶解速率;在量取蒸馏水读数时,视线如图2所示(其他操作正确),会造成所配制溶液的溶质质量分数偏小(填“偏大”、“偏小”、“无影响”).
分析 (1)根据溶质质量=溶液质量×溶质的质量分数,进行分析判断.
(2)根据托盘天平的使用要遵循“左物右码”的原则、氢氧化钠具有腐蚀性,进行分析判断.
(3)根据操作②溶解操作中玻璃棒的作用,图2用量筒量取水时,仰视液面,读数比实际液体体积小,进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为10%的氢氧化钠溶液,需氢氧化钠的质量=100g×10%=10g.
(2)托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量.
(3)操作②溶解操作中玻璃棒的作用搅拌,加快溶解速率.
图2用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
故答案为:(1)10;(2)C;(3)搅拌,加快溶解速率;偏小.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
16.人体内的一些液体的pH值如下,其中酸性最强的是( )
| A. | 唾液 pH=6.7 | B. | 胆汁 pH=7.2 | C. | 胃液 pH=1.0 | D. | 血液 pH=7.4 |
9.根据自己的经验,判断新鲜杨梅汁是( )
| A. | 酸性的 | B. | 碱性的 | C. | 中性的 | D. | 都有可能 |
10.日常生活中下列做法,可以用物质化学性质解释的是( )
| A. | 用油做润滑剂 | B. | 用汽油洗掉衣服上的油污 | ||
| C. | 用纯碱除去面团因发酵产生的酸味 | D. | 用木炭粉除去冰箱内的异味 |