题目内容
14.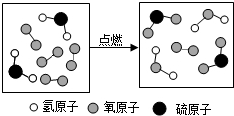 如图是某反应的微观示意图,下列说法不正确的是( )
如图是某反应的微观示意图,下列说法不正确的是( )| A. | 反应物中有单质 | B. | 该反应前后分子个数不变 | ||
| C. | 生成物的分子个数比为1:1 | D. | 参加反应的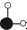 和 和 的质量比为17:24 的质量比为17:24 |
分析 根据反应过程图中的分子结构,判断反应物与生成物,确定该反应中各分子个数比和反应的化学方程式,据此分析解答.
解答 解:由图示可知反应前后存在相同的分子,故该图示可转化为如图的反应图示:
依据反应前后物质的分子结构可知反应物是氧气和硫化氢生成物是水和二氧化硫,则反应方程式为3O2+2H2S$\frac{\underline{\;点燃\;}}{\;}$2H2O+2SO2;
A、单质是由一种元素组成的纯净物,化合物是由多种元素组成的纯净物,故反应物中氧气属于单质,硫化氢属于化合物,故说法正确;
B、观察方程式可知,反应前分子的个数是5个,而反应后是4个,故说法错误;
C、由图示或化学方程式都可以看出生成物的分子个数比是1:1,故说法正确;
D、根据化学方程式可知,常见反应的硫化氢和氧气的质量比为2×34:3×32=17:24,故说法正确.
故选B.
点评 该题不仅考查了学生对化学知识的掌握情况,还考查了学生观察理解微观模型示意图的能力,从多方面考查了学生的综合能力,根据微观示意图写出反应的方程式即可迅速分析判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.二氧化硫、氧气、氧化铜含有相同的( )
| A. | 氧气 | B. | 氧元素 | C. | 氧分子 | D. | 两种元素 |
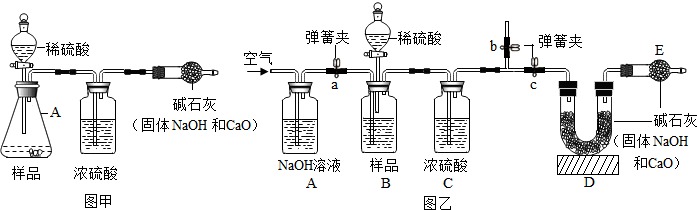
5. 一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:
一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:
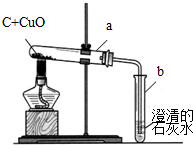
通过实验及分析,确定该粉末为氧化铜和碳粉混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验:
①试管a中的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
②氧化铜和碳反应属于置换反应.(填基本反应类型)
③最能说明a试管中氧化铜和碳已完全反应的实验现象是b中的导管口不再产生气泡(合理即可).
 一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:
一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含C |
①试管a中的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
②氧化铜和碳反应属于置换反应.(填基本反应类型)
③最能说明a试管中氧化铜和碳已完全反应的实验现象是b中的导管口不再产生气泡(合理即可).
6.分别在冷水和热水中同时注入一滴墨水,5s后的现象如图所示,该现象说明( )

| A. | 只有热水的分子在做热运动 | |
| B. | 热水有内能,冷水没有内能 | |
| C. | 温度越高,分子运动越剧烈 | |
| D. | 扩散只能在液体中发生,不能在气体、固体中发生 |
3.小明用量筒量取液体,量筒平稳且面对刻度线,初次视线与量筒内液体的凹液面最低处保持水平,读书为16mL,取出部分液体后仰视凹液面最低处,读数为12mL,则小明实际取出的液体体积为( )
| A. | 小于4mL | B. | 等于4mL | ||
| C. | 大于4mL | D. | 可能大于4mL,也可能小于4mL |
2.下列说法正确的是( )
| A. | 蜡烛燃烧后,越来越短、最终消失,能够用质量守恒定律来解释 | |
| B. | 根据质量守恒定律,1g氢气与1g氧气反应能生成2g水 | |
| C. | 5g水蒸发得到5g水蒸气,这很好的说明了质量守恒定律 | |
| D. | 铁丝在氧气中燃烧,生成四氧化三铁的质量等于反应前物质的质量和 |
 Mg2+.
Mg2+.