题目内容
15. 图中A、B、C、D、E是初中化学常见的五种不同类别的物质,A是产量最大的一种金属,E是导致温室效应的一种气体,图中“--”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).
图中A、B、C、D、E是初中化学常见的五种不同类别的物质,A是产量最大的一种金属,E是导致温室效应的一种气体,图中“--”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).(1)A易锈蚀生成红褐色的物质其化学式Fe2O3,写出物质E的一种用途灭火.
(2)物质C与E反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(3)写出图中一个属于中和反应的化学方程式2NaOH+H2SO4═Na2SO4+2H2O.
分析 根据A、B、C、D、E是初中化学常见的五种不同类别的物质,A是产量最大的一种金属,所以A是铁,E是导致“温室效应”的一种气体,所以E是二氧化碳,二氧化碳能够和碱溶液反应,所以C可以是氢氧化钠等碱溶液,氢氧化钠等碱溶液还能够和酸、某些盐溶液反应,因此B可以是酸,如硫酸;B能够转化为D,则D可能是盐溶液,A能够和B-酸、D-盐反应,则D可以是硫酸铜,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E是初中化学常见的五种不同类别的物质,A是产量最大的一种金属,所以A是铁,E是导致“温室效应”的一种气体,所以E是二氧化碳,二氧化碳能够和碱溶液反应,所以C可以是氢氧化钠等碱溶液,氢氧化钠等碱溶液还能够和酸、某些盐溶液反应,因此B可以是酸,如硫酸;B能够转化为D,则D可能是盐溶液,A能够和B-酸、D-盐反应,则D可以是硫酸铜,经过验证,推导正确,所以A易锈蚀生成红褐色的物质其化学式是Fe2O3,E是二氧化碳,可以用来灭火;
(2)C是碱溶液,如氢氧化钠,与二氧化碳反应产生碳酸钠和水,化学方程式为:CO2+2NaOH=Na2CO3+H2O;
(3)中和反应是酸和碱之间的反应,因此是B和C反应,如硫酸和氢氧化钠反应产生硫酸钠和水,化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O.
故答案为:(1)Fe2O3,灭火;
(2)CO2+2NaOH=Na2CO3+H2O;
(3)2NaOH+H2SO4═Na2SO4+2H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
6.对下列微粒的叙述是正确的是( )
| A. | 物质都是由分子组成的 | |
| B. | 分子在不断的运动,原子不动 | |
| C. | 原子中质子数等于电子数 | |
| D. | 原子失去了电子,带负电荷,成为阴离子 |
20.把少量的下列物质分别放入水中,充分搅拌后,可以得到溶液的是( )
| A. | 面粉 | B. | 植物油 | C. | 汽油 | D. | 氯化钠 |
7. 如图所示装置可用于洗气、集气、验气和储气等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )
如图所示装置可用于洗气、集气、验气和储气等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )
 如图所示装置可用于洗气、集气、验气和储气等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )
如图所示装置可用于洗气、集气、验气和储气等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )| A. | 瓶中装有适量的NaOH溶液,除去氢气中含有的少量二氧化碳气体 | |
| B. | 瓶中装满水,用排水集气法收集氧气 | |
| C. | 瓶中装有澄清石灰水,检验一氧化碳气体中是否混有二氧化碳 | |
| D. | 瓶中装有氧气,将水从导气管通入以取用瓶内储存的气体 |
4.关于某溶液所含离子检验的方法和结论正确的是( )
| A. | 加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定含有NH4+ | |
| B. | 加入盐酸产生能使澄清石灰水变浑浊的无色气体,则原溶液中一定含有CO32- | |
| C. | 加入AgNO3溶液有白色沉淀生成,再加稀盐酸沉淀不消失,则原溶液一定含有Cl- | |
| D. | 加入NaOH溶液,有白色沉淀生成,则原溶液一定含有Al3+ |
5.现有下列物质属于混合物的是( )
| A. | 蒸馏水 | B. | 冰水混合物 | C. | 液态空气 | D. | 干冰 |
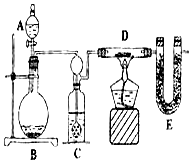 某同学为了测定水中氢、氧两元素的质量比,设计了以下实验,实验装置如图.
某同学为了测定水中氢、氧两元素的质量比,设计了以下实验,实验装置如图.