题目内容
16.某课外活动小组为了测定铜锌合金中铜的质量分数,取铜锌合金样品20g,将100g稀硫酸加入样品中,使样品充分反应,直至无气泡产生,称得反应后剩余物质的总质量为119.6g,请回答下列问题:(1)产生氢气的质量0.4g.
(2)求铜锌合金中铜的质量分数是多少?
分析 锌和稀硫酸反应生成硫酸锌和氢气,反应前后的质量差即为反应生成氢气质量,根据提供的数据可以进行相关方面的计算.
解答 解:(1)生成氢气质量为:20g+100g-119.6g=0.4g,
故填:0.4g.
(2)设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.4g
$\frac{65}{x}$=$\frac{2}{0.4g}$,
x=13g,
铜锌合金中铜的质量分数为:$\frac{20g-13g}{20g}$×100%=35%,
答:铜锌合金中铜的质量分数为35%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
15.下列各组物质中,能相互反应且反应前后溶液总质量保持不变的是( )
| A. | 铝和硫酸铜溶液 | B. | 二氧化碳和石灰水 | ||
| C. | 硫酸和烧碱溶液 | D. | 氧化铁固体和盐酸 |
4.下列物质分别加入水中充分搅拌,不能得到溶液的是( )
| A. | 食盐 | B. | 硫酸铜 | C. | 植物油 | D. | 氢氧化钠 |
11.下列变化属于化学变化的是( )
| A. | 自行车轮胎爆炸 | B. | 石油的炼制 | ||
| C. | 煤的综合利用 | D. | 分离液态空气制氧气 |
1.我国科学家屠呦呦发现了青蒿素(青蒿素的化学式:C15H22O5),获得2015年诺贝尔医学奖,它是一种用于治疗疟疾的药.下列关于青蒿素的说法正确的是( )
| A. | 该物质由三个元素组成 | |
| B. | 该物质中碳、氢、氧元素的质量比为15:22:5 | |
| C. | 该物质中氢元素的质量分数最小 | |
| D. | 其分子由碳原子、氢元素和氧分子构成 |
6.下列有关燃烧与灭火的说法中,正确的是( )
| A. | 水能灭火主要是因为水蒸发吸热,降低了可燃物的着火点 | |
| B. | 白磷在冷水中,通入空气后也能燃烧 | |
| C. | 将煤制成“蜂窝煤”是为了增大煤与空气的接触面积,使其燃烧更充分 | |
| D. | 燃烧一定会引起爆炸 |
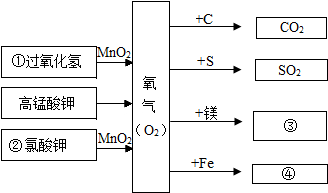 如图有关氧气的知识网络图(反应条件部分省略),用化学用语回答:
如图有关氧气的知识网络图(反应条件部分省略),用化学用语回答: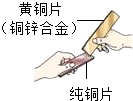 金属材料在人类活动中已得到越来越广泛的应用.
金属材料在人类活动中已得到越来越广泛的应用.