题目内容
7.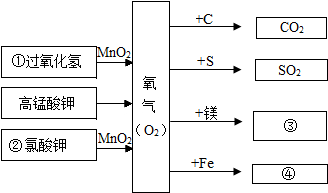 如图有关氧气的知识网络图(反应条件部分省略),用化学用语回答:
如图有关氧气的知识网络图(反应条件部分省略),用化学用语回答:(1)物质①的4个分子4H2O2;
(2)物质②的阳离子是K+;
(3)物质③的化学式,并标出金属元素的化合价$\stackrel{+2}{Mg}$O;
(4)生成物质④的化学方程式Fe3O4.
分析 每个过氧化氢分子由2个氢原子和2个氧原子构成;
氯酸钾中的阳离子是钾离子,每个钾离子带1个单位正电荷;
镁在氧气中燃烧生成氧化镁,氧化镁中,镁元素的化合价是+2;
铁在氧气中燃烧生成四氧化三铁.
解答 解:(1)4个过氧化氢分子可以表示为4H2O2;
(2)物质②的阳离子是钾离子,可以表示为K+;
(3)物质③是氧化镁,其中镁元素的化合价是+2,可以表示为$\stackrel{+2}{Mg}$O;
(4)生成物质④是四氧化三铁,可以表示为Fe3O4.
故填:4H2O2;K+;$\stackrel{+2}{Mg}$O;Fe3O4.
点评 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
6.关子①海水②氧气③汞④澄清的石灰水⑤硫酸铜⑥五氧化二磷⑦蒸馏水,7种物质的分类正确的是( )
| A. | ①④⑦为混合物 | B. | ④⑤为化合物 | C. | ⑤⑥⑦为氧化物 | D. | ②③为单质 |
7.小华在一次探究实验中将一小粒金属钠投入盛有蒸馏水的烧杯中,发现反应剧烈并生成大量气体,根据所学知识推断则该气体可能是( )
| A. | H2 | B. | CH4 | C. | He | D. | NH3 |
4. 在实验室中称取24g小苏打样品(所含杂质不与盐酸反应),平均分成5份依次加入到盛有50g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后进行称量,得到的一些实验数据如表:
在实验室中称取24g小苏打样品(所含杂质不与盐酸反应),平均分成5份依次加入到盛有50g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后进行称量,得到的一些实验数据如表:
(1)第三次加入样品后,生成挥发性物质小于(填“大于”或“小于”)第二次,原因是第三次加入的碳酸氢钠没有完全反应;
(2)样品中碳酸氢钠的质量分数为87.5%;
(3)所用稀盐酸的质量分数为9.1%.
 在实验室中称取24g小苏打样品(所含杂质不与盐酸反应),平均分成5份依次加入到盛有50g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后进行称量,得到的一些实验数据如表:
在实验室中称取24g小苏打样品(所含杂质不与盐酸反应),平均分成5份依次加入到盛有50g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后进行称量,得到的一些实验数据如表:| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入样品的质量/g | 4.8 | 4.8 | 4.8 | 4.8 | 4.8 |
| 电子天平的示数/g | 112.6 | 115.2 | 118.9 | 123.7 | 128.5 |
| 生成挥发性物质的质量/g |
(2)样品中碳酸氢钠的质量分数为87.5%;
(3)所用稀盐酸的质量分数为9.1%.
2.水是生命之源.下面有关水的叙述中,正确的是( )
| A. | 电解水的实验证明了水是由氢气和氧气组成的 | |
| B. | 过滤可以将硬水转化成软水 | |
| C. | 原子是化学变化中的最小微粒,原子一定是由质子、中子和电子构成的 | |
| D. | 净化水的方法中,蒸馏是单一净化程度最高的方法 |
