题目内容
14.比较和归纳是学习化学的常用方法.某学习小组的同学在下图所列出的实验装置的基础上,对气体的制取进行研究.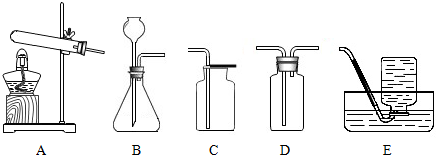
(1)确定气体发生装置应考虑的因素是反应物的状态和反应条件.
(2)实验室用加热高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验室可选用的发生装置为A,可选用的收集装置为C或D或E.
(3)甲同学用大理石与稀盐酸反应制取二氧化碳气体,化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;要得到一瓶干燥的二氧化碳气体,所选装置的连接顺序是B→D→C(填字母),可选用浓硫酸作干燥剂.
(4)加热固体碳酸氢钠或固体碳酸氢铵都能产生二氧化碳气体,化学反应方程式分别是:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑;NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+H2O+CO2↑
乙同学选择加热碳酸氢钠的反应制取二氧化碳,则发生装置应选用A(填字母).他不选择加热碳酸氢铵制取二氧化碳的理由是碳酸氢铵受热分解生成二氧化碳,同时生成氨气.
分析 (1)根据不同的实验装置,功能不同进行分析;
(2)根据高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气进行分析;
根据氧气的密度比空气大,不易溶于水进行分析;
(3)根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能够溶于水,密度比空气大;浓硫酸具有吸水性,可以用作某些物质的干燥剂进行分析;
(4)根据物质反应生成物的状态可以选择适合制取气体的反应物.
解答 解:(1)确定气体发生装置应考虑的因素是反应物状态和反应条件;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
利用高锰酸钾制取氧气时需要加热,应该用A装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用C或D装置收集,氧气不易溶于水,可以用排水法收集,即用E装置收集;
(3)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
要得到一瓶干燥的二氧化碳气体,所选装置的连接顺序是:反应不需要加热,应该用B装置作为发生装置,从B装置导出的二氧化碳应该导入D装置中,D装置中可以盛放浓硫酸,用来干燥二氧化碳,二氧化碳导出后,再用C装置收集;
(4)利用碳酸氢钠反应制取二氧化碳时需要加热,则发生装置应选用A装置;
因为碳酸氢铵受热分解生成二氧化碳,同时生成氨气,会导致收集的二氧化碳不纯,所以不选择加热碳酸氢铵制取二氧化碳.
故答案为:(1)反应物状态,反应条件;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,A,C或D或E;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑,B→D→C,浓硫酸;
(4)A,碳酸氢铵受热分解生成二氧化碳,同时生成氨气.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】(A)溶质可能是CaCl2与Ca(OH)2 (B)溶质可能是CaCl2 (C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液与试管中,逐滴加入碳酸钠溶液 | 产生沉淀 | 猜想(B)正确 |
| 先产生气泡,后产生沉淀 | 猜想(C)正确 |
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀铁质下水道
水污染,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的石灰石,充分反应后过滤,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
| A. | 偏二甲肼是一种氧化物 | |
| B. | 偏二甲肼由碳、氢、氮三种元素组成 | |
| C. | 偏二甲肼由12个原子构成 | |
| D. | 偏二甲肼中碳元素的质量分数为10% |
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有A.
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液 )
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH;④…..
【实验验证】(提示CaCl2溶液显中性)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 有白色沉淀产生 溶液仍为红色 | 猜想③成立 |
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】
①该氢氧化钠溶液没有变质;②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸根离子(或碳酸钠) | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀.静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.