题目内容
9.下列试剂中不能够将KNO3、Ba(OH)2、稀盐酸三种无色溶液鉴别出来的是( )| A. | 紫色石蕊试液 | B. | K2CO3溶液 | C. | Na2SO4溶液 | D. | Cu(OH)2固体 |
分析 根据KNO3、Ba(OH)2、稀盐酸的性质进行分析,能够将KNO3、Ba(OH)2、稀盐酸三种无色溶液鉴别出来的试剂是遇到三种试剂能够呈现不同现象即可.
解答 解:A、分别滴入石蕊,变红的是稀盐酸,变蓝的是氢氧化钡溶液,不变色的是硝酸钾溶液,可以鉴别出来,故A正确;
B、将K2CO3溶液分别滴入KNO3、Ba(OH)2、稀盐酸三种无色溶液中,有沉淀的是氢氧化钡,有气体的是稀盐酸,无现象的是硝酸钾,故B正确;
C、Na2SO4溶液与Ba(OH)2反应生成白色沉淀,不能与KNO3、稀盐酸反应,无法将剩余无色溶液鉴别出来,故C错误;
D、Cu(OH)2固体与Ba(OH)2混合无现象,与KNO3溶液混合无现象,稀盐酸混合沉淀消失,溶液变蓝,无法将氢氧化钡溶液和硝酸钾溶液鉴别出来,故D错误.
故选CD.
点评 通过回答本题知道了鉴别物质的方法是加入一种试剂,所呈现的现象不一样就可以鉴别开.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
7.化学实验是学习化学的基础,请根据下列装置图回答问题.
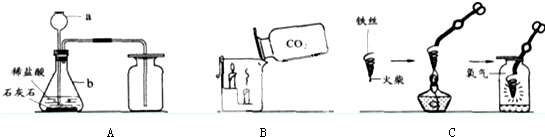
(1)写出仪器a、b的名称长颈漏斗;b锥形瓶.
(2)写出A图中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层先灭,说明二氧化碳具有不能燃烧、不支持燃烧和密度比空气大性质.这一性质在实际生活中的应用为灭火.
(4)C图中螺旋状铁丝的末端系一根火柴的作用是引燃铁丝.
(5)小明按C图实验时,集气瓶炸裂了,其可能的原因是燃着的铁丝碰到集气瓶壁.
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
铁丝在氧气中燃烧产生火星四射的原因是碳与氧气或熔融状态的铁的氧化物反应生成二氧化碳气体,二氧化碳气体体积迅速膨胀,推动周围的呈熔融状态的铁及其氧化物向四周飞溅.

(1)写出仪器a、b的名称长颈漏斗;b锥形瓶.
(2)写出A图中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层先灭,说明二氧化碳具有不能燃烧、不支持燃烧和密度比空气大性质.这一性质在实际生活中的应用为灭火.
(4)C图中螺旋状铁丝的末端系一根火柴的作用是引燃铁丝.
(5)小明按C图实验时,集气瓶炸裂了,其可能的原因是燃着的铁丝碰到集气瓶壁.
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 剧烈燃烧,大量火星 |
4.小明在做“酸碱中和反应”实验时,向盛有氢氧化钠溶液的烧杯中滴入几滴酚酞溶液,观察到溶液变红,接着,他又向其中加入一定量稀硫酸,发现红色褪去.
【提出问题】反应后所得溶液中溶质是什么?
【提出猜想】化学兴趣小组同学根据上述实验现象,一致认为反应后溶液中的溶质(除酚酞溶液外)一定有Na2SO4,理由是2NaOH+H2SO4=Na2SO4+2H2O(用化学方程式表示).
【设计方案】小红经过认真分析,认为反应后所得的溶液中还可能存在硫酸,并针对自己的猜想,设计了下列两种实验方案:
【反思评价】小组同学仔细研究上述两种实验方案后,认为方案1无法验证小红猜想的正确性,理由是硫酸钠和硫酸都能与硝酸钡溶液反应,生成白色沉淀,无法确定溶液中是否含有硫酸
【拓展迁移】大家讨论后,按正确方案进行操作,确认了溶液中有硫酸存在,由此可知,在分析化学反应结束后所得物质的成分时,除了要考虑到生成物外,还要考虑到反应物是否过量.若反应所得溶液的PH=7,此时溶液中大量存在的粒子有Na+\SO42-H2O.
【提出问题】反应后所得溶液中溶质是什么?
【提出猜想】化学兴趣小组同学根据上述实验现象,一致认为反应后溶液中的溶质(除酚酞溶液外)一定有Na2SO4,理由是2NaOH+H2SO4=Na2SO4+2H2O(用化学方程式表示).
【设计方案】小红经过认真分析,认为反应后所得的溶液中还可能存在硫酸,并针对自己的猜想,设计了下列两种实验方案:
| 实验方案 | 实验步骤 | 预期现象 | 结论 |
| 方案1 | 取样,滴入适量的硝酸钡溶液 | 出现白色沉淀 | 有硫酸 |
| 方案2 | 取样,滴入盛有锌粒的试管中 | 出现气泡 | 有硫酸 |
【拓展迁移】大家讨论后,按正确方案进行操作,确认了溶液中有硫酸存在,由此可知,在分析化学反应结束后所得物质的成分时,除了要考虑到生成物外,还要考虑到反应物是否过量.若反应所得溶液的PH=7,此时溶液中大量存在的粒子有Na+\SO42-H2O.
 金属和酸、碱、盐的化学性质是初中化学的核心知识,如图,A、B、C、D分别表示上述四类物质中常见的一种,A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能够发生中和反应,B可以用来改良酸性土壤,D是目前世界上产量最多的金属.请回答:
金属和酸、碱、盐的化学性质是初中化学的核心知识,如图,A、B、C、D分别表示上述四类物质中常见的一种,A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能够发生中和反应,B可以用来改良酸性土壤,D是目前世界上产量最多的金属.请回答: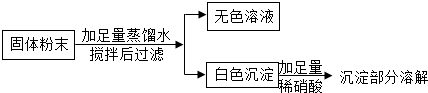
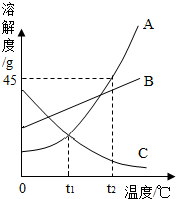 如图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题: