��Ŀ����
�����Ƹ�����ͭ��Һ�������·�Ӧ��2Na+2H2O+CuSO4==Na2SO4+Cu(OH)2��+H2������73.7g����ͭ��Һ�м���2.3g�ƣ�ǡ�÷�Ӧ��ȫ���Լ��㣺
(1)���ɳ�����������������Ϊ���ٿˣ�
(2)��Ӧֹͣ����ȥ������������Һ�����ʵ����������Ƕ��٣�
(3)��˼��ѧϰ��һ����Ҫ���������ݽ����Ƹ�����ͭ��Һ������Ӧ��ʵ�ʣ���Խ������˳������⽫�������̣���̸һ̸��Խ������˳����õ���ʶ�� ��
(1)���ɳ�����������������Ϊ���ٿˣ�
(2)��Ӧֹͣ����ȥ������������Һ�����ʵ����������Ƕ��٣�
(3)��˼��ѧϰ��һ����Ҫ���������ݽ����Ƹ�����ͭ��Һ������Ӧ��ʵ�ʣ���Խ������˳������⽫�������̣���̸һ̸��Խ������˳����õ���ʶ�� ��
�⣺��1��������ͭ��Һ������ȫ��Ӧ�����������ơ������������������ֱ�Ϊ��x��y��z
2Na+2H2O + CuSO4==Na2SO4+Cu(OH)2��+H2��
46 142 98 2
2.3g x y z
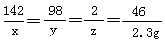
x=7.1g
y=4.9g
z=0.1g
�����ɳ�����������������Ϊ��4.9g��0.1g
��2����Ӧֹͣ����ȥ������������Һ�����ʵ���������Ϊ��
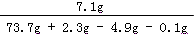 ��100%=10%
��100%=10%
�𣺷�Ӧֹͣ����ȥ������������Һ�����ʵ����������ǣ�10%
��3���ڽ������˳���У�����ǰ��Ľ�����һ���ܰѺ���Ľ�����������Һ���û�������ֻҪ�ܴ����������������Һ��Ӧ��صĺ����𰸶����ԣ�
2Na+2H2O + CuSO4==Na2SO4+Cu(OH)2��+H2��
46 142 98 2
2.3g x y z
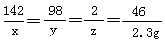
x=7.1g
y=4.9g
z=0.1g
�����ɳ�����������������Ϊ��4.9g��0.1g
��2����Ӧֹͣ����ȥ������������Һ�����ʵ���������Ϊ��
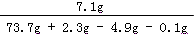 ��100%=10%
��100%=10%�𣺷�Ӧֹͣ����ȥ������������Һ�����ʵ����������ǣ�10%
��3���ڽ������˳���У�����ǰ��Ľ�����һ���ܰѺ���Ľ�����������Һ���û�������ֻҪ�ܴ����������������Һ��Ӧ��صĺ����𰸶����ԣ�

��ϰ��ϵ�д�
 ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д�
�����Ŀ

 ����74.24g����ͭ��Һ�м���2.76g�ƣ�ǡ�÷�Ӧ��ȫ���ܼ�ˮ��ʣ�ࣩ���Լ��㣺
����74.24g����ͭ��Һ�м���2.76g�ƣ�ǡ�÷�Ӧ��ȫ���ܼ�ˮ��ʣ�ࣩ���Լ��㣺