题目内容
16. 铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:Ⅰ.铜绿的主要成分是碱式碳酸铜:Cu2(OH)2CO3.
Ⅱ.铜器因所处环境不同,生成的铜绿中可能还含有CuSO4和CuC12.
Ⅲ.硫酸铜、氯化铜的化学性质稳定,酒精灯加热条件下不分解.
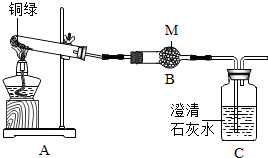
为了探究碱式碳酸铜的化学性质,该小组同学取少量铜绿(假设杂质不参与反应)按如图装置进行实验:
(1)M药品的名称是无水硫酸铜.
(2)实验过程中,发现A中绿色固体逐渐变为黑色,B中固体变蓝色,C中溶液变浑浊.写出Cu2(OH)2CO3分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(3)为了验证铜绿中是否有CuSO4和CuC12,该小组同学进行了如下实验,请补充完成下列实验报告:
| 步骤 | 操作 | 现象及结论 |
| ① | 取少量铜绿溶于足量稀硝酸中,并将溶液分成甲、乙两份 | 产生气泡 |
| ② | 向甲中滴加硝酸钡溶液 | 若观察到 产生白色沉淀,则铜绿中含有CuSO4 |
| ③ | 向乙中加入过量的硝酸钡溶液,振荡、静置,取上层清液于试管中,再滴加硝酸银溶液 | 若观察到产生白色沉淀,则铜绿中含有CuCl2 |
分析 无水硫酸铜是白色固体,能和水反应生成蓝色五水硫酸铜;
碱式碳酸铜受热分解生成氧化铜、水和二氧化碳;
硝酸钡和硫酸铜反应生成硫酸钡沉淀和硝酸铜,硫酸钡不溶于稀硝酸;
硝酸银和氯化铜反应生成氯化银沉淀和硝酸铜,氯化银不溶于稀硝酸.
解答 解:(1)M药品的名称是无水硫酸铜,五水硫酸铜能和水反应生成蓝色五水硫酸铜晶体,因此无水硫酸铜可以检验是否生成水.
故填:无水硫酸铜.
(2)实验过程中,发现A中绿色固体逐渐变为黑色,说明生成了氧化铜,B中固体变蓝色,说明生成了水,C中溶液变浑浊,说明生成的二氧化碳,Cu2(OH)2CO3分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
故填:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(3)为了验证铜绿中是否有CuSO4和CuC12,该小组同学进行了如下实验,完成实验报告如下表所示:
| 步骤 | 操作 | 现象及结论 |
| ① | 取少量铜绿溶于足量稀硝酸中,并将溶液分成甲、乙两份 | 产生气泡 |
| ② | 向甲中滴加硝酸钡溶液 | 若观察到产生白色沉淀,则铜绿中含有 CuSO4 |
| ③ | 向乙中加入过量的硝酸钡溶液,振荡、静置,取上层清液于试管中,再滴加硝酸银溶液 | 若观察到产生白色沉淀,则铜绿中含有 CuC12 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
5.2011年正月初一,宜春市空气污染指数飙升,空气污染指数为311,其首要污染物为可吸入颗粒物和二氧化硫.请你回答下列问题:
(1)以下是空气污染指数与质量级别、质量状况的对应关系:
根据以上信息,判断宜春市当天的空气质量级别和空气质量状况分别是D
A.I级 优B.II级 良 C.III级 轻度污染D.V级 重度污染
(2)当天空气中二氧化硫和可吸入颗粒物的来源主要是③(填序号);
①大扫除的家庭增多;②植物的呼吸作用;③大量燃放烟花、鞭炮;④工厂大量燃烧煤
(3)为提高宜春市的空气质量,请提出两条切实可行的建议:①严禁燃放烟花、鞭炮,②将燃煤改为燃气等.
(1)以下是空气污染指数与质量级别、质量状况的对应关系:
| 空气污染指数 | 0~50 | 51~100 | 101~200 | 201~300 | >300 |
| 空气质量状况 | 优 | 良 | 轻度污染 | 中度污染 | 重度污染 |
| 空气质量级别 | I | II | III | IV | V |
A.I级 优B.II级 良 C.III级 轻度污染D.V级 重度污染
(2)当天空气中二氧化硫和可吸入颗粒物的来源主要是③(填序号);
①大扫除的家庭增多;②植物的呼吸作用;③大量燃放烟花、鞭炮;④工厂大量燃烧煤
(3)为提高宜春市的空气质量,请提出两条切实可行的建议:①严禁燃放烟花、鞭炮,②将燃煤改为燃气等.
4.下列有关溶液的说法正确的是( )
| A. | 透明的溶液一定不含氯化铁、硫酸铜、高锰酸钾 | |
| B. | 均一、稳定的液体一定是溶液 | |
| C. | 溶液是混合物,至少由两种物质组成 | |
| D. | 固体与气体反应一般比溶液与气体反应快 |
1.检验碳酸盐的试剂是( )
| A. | 紫色石蕊试液 | B. | 无色酚酞试液 | C. | 盐酸和石灰水 | D. | 盐酸 |


 如图是初中化学中的一些重要实验.请回答:
如图是初中化学中的一些重要实验.请回答: