题目内容
1.检验碳酸盐的试剂是( )| A. | 紫色石蕊试液 | B. | 无色酚酞试液 | C. | 盐酸和石灰水 | D. | 盐酸 |
分析 A、根据酸碱指示剂一般检验溶液的酸碱性进行分析;
B、根据酸碱指示剂一般检验溶液的酸碱性进行分析;
C、根据碳酸盐会与盐酸反应生成二氧化碳气体,石灰水是检验二氧化碳气体的存在的进行分析;
D、根据碳酸盐和盐酸反应会产生气体进行分析.
解答 解:A、虽然石蕊遇碱会变蓝色,有的碳酸盐显碱性,但是不是所有的碳酸盐都会溶于水,故A错误,
B、虽然酚酞遇碱会变蓝色,有的碳酸盐显碱性,但是不是所有的碳酸盐都会溶于水,比如碳酸钙就不会使酚酞变红色,故B错误,
C、在固体中加入盐酸会产生气体,然后将气体通入澄清石灰水中会生成沉淀,气体就是二氧化碳,也就检验了碳酸盐的存在,故C正确;
D、在固体中加入盐酸会产生气体的,不一定只有碳酸盐,也有活泼的金属,比如:铁,故D错误.
故选C.
点评 在解此类题时,首先分析需要鉴别物质的性质,然后选择的试剂要出现一定特有的现象才能鉴别.

练习册系列答案
相关题目
10.下列是生产、生活中常用的物质,其中属于混合物的是( )
| A. | 冰水 | B. | 高锰酸钾 | C. | 液氮 | D. | 空气 |
12.从分子和原子的角度分析并解释下列事实,其中不正确的是( )
| A. | 物体的热胀冷缩--分子的体积发生变化 | |
| B. | 品红在水中扩散--分子在不断运动 | |
| C. | 氧化汞分解成汞和氧气--分子可以再分 | |
| D. | 一滴水中大约有1.67×1021个水分子--分子很小 |
16.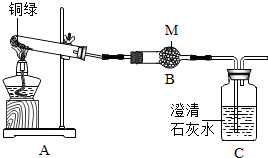 铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
Ⅰ.铜绿的主要成分是碱式碳酸铜:Cu2(OH)2CO3.
Ⅱ.铜器因所处环境不同,生成的铜绿中可能还含有CuSO4和CuC12.
Ⅲ.硫酸铜、氯化铜的化学性质稳定,酒精灯加热条件下不分解.
为了探究碱式碳酸铜的化学性质,该小组同学取少量铜绿(假设杂质不参与反应)按如图装置进行实验:
(1)M药品的名称是无水硫酸铜.
(2)实验过程中,发现A中绿色固体逐渐变为黑色,B中固体变蓝色,C中溶液变浑浊.写出Cu2(OH)2CO3分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(3)为了验证铜绿中是否有CuSO4和CuC12,该小组同学进行了如下实验,请补充完成下列实验报告:
 铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:Ⅰ.铜绿的主要成分是碱式碳酸铜:Cu2(OH)2CO3.
Ⅱ.铜器因所处环境不同,生成的铜绿中可能还含有CuSO4和CuC12.
Ⅲ.硫酸铜、氯化铜的化学性质稳定,酒精灯加热条件下不分解.
为了探究碱式碳酸铜的化学性质,该小组同学取少量铜绿(假设杂质不参与反应)按如图装置进行实验:
(1)M药品的名称是无水硫酸铜.
(2)实验过程中,发现A中绿色固体逐渐变为黑色,B中固体变蓝色,C中溶液变浑浊.写出Cu2(OH)2CO3分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(3)为了验证铜绿中是否有CuSO4和CuC12,该小组同学进行了如下实验,请补充完成下列实验报告:
| 步骤 | 操作 | 现象及结论 |
| ① | 取少量铜绿溶于足量稀硝酸中,并将溶液分成甲、乙两份 | 产生气泡 |
| ② | 向甲中滴加硝酸钡溶液 | 若观察到 产生白色沉淀,则铜绿中含有CuSO4 |
| ③ | 向乙中加入过量的硝酸钡溶液,振荡、静置,取上层清液于试管中,再滴加硝酸银溶液 | 若观察到产生白色沉淀,则铜绿中含有CuCl2 |
6.以下符号书写错误的是( )
| A. | 三个氢原子:H3 | B. | 两个氮分子:2N2 | ||
| C. | 一个二氧化碳分子:CO2 | D. | 四个镁离子:4Mg2+ |
13.下列鉴别物质所用的方法或试剂,错误的是( )
| A. | 氧气和氮气--观察颜色 | B. | 铁粉和炭粉--用磁铁 | ||
| C. | 氧气和二氧化碳一-带火星的木条 | D. | 硬水和软水--用肥皂水 |
 .
.
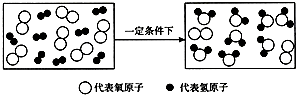 如图是某化学变化的微观示意图.
如图是某化学变化的微观示意图.