题目内容
11.科学合理膳食,能够使人体中各种元素形成“收支平衡”,以保障健康.下列属于人体中微量元素的是点燃( )
| A. | 铁 | B. | 氧 | C. | 钙 | D. | 氢 |
分析 根据常量元素与微量元素的区别和种类进行分析判断即可.
解答 解:在人体内含量大于00.1%的是常量元素,否则属于微量元素,人体内的常量元素主要有:氧、碳、氢、氮、钙、磷、钾、硫、钠、氯、镁;微量元素主要有:铁、钴、铜、锌、铬、锰、钼、氟、碘、硒.
故选A.
点评 本题考查微量元素的种类,难度不大,掌握常量元素与微量元素的种类即可正确解答此类问题.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案
相关题目
6.下列化学符号书写不正确的是( )
| A. | 氖气:Ne2 | B. | 氨分子:NH3 | C. | 硅原子:Si | D. | 亚铁离子:Fe2+ |
16.类推是一种重要的学习方法,下列类推结论正确的是( )
| A. | 乙酸铅能使蛋白质失去生理活性,硫酸铵也能使蛋白质失去生理活性 | |
| B. | NaCl溶于水溶液温度无明显变化,则NH4NO3溶于水溶液温度也无明显变化 | |
| C. | 点燃H2与O2混合气体可能爆炸,则点燃CO与O2的混合气体也可能爆炸 | |
| D. | CuO不能与水反应,则CaO也不能与水反应 |
3. 现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.
现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.
【猜想假设】猜想一:没有变质,为NaOH溶液;猜想二:全部变质,为Na2CO3溶液.
猜想三:该溶液部分变质,为NaOH、Na2CO3溶液.
【查阅资料】Na2CO3溶液呈碱性,CaCl2溶液呈中性.
【设计方案】请你完善下表几组同学探讨的设计方案.
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
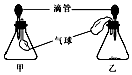
【拓展延伸】同学们设计了如图两套装置进行实验:用胶头滴管吸取某种液体,锥形瓶中充入一种气体或
放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
(1)若甲中充入的气体是CO2,则可能发生反应的方程式CO2+2NaOH═Na2CO3+H2O.(任写一个)
(2)若乙中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是铁.(任写一种)
 现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.
现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.【猜想假设】猜想一:没有变质,为NaOH溶液;猜想二:全部变质,为Na2CO3溶液.
猜想三:该溶液部分变质,为NaOH、Na2CO3溶液.
【查阅资料】Na2CO3溶液呈碱性,CaCl2溶液呈中性.
【设计方案】请你完善下表几组同学探讨的设计方案.
| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 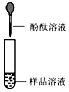 | 溶液变红,则猜想一成立. | 第2组同学认为:此方案结论不正确,理由 是:碳酸钠溶液显碱性,也能使酚酞试液变红色. |
| 第2组 | 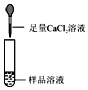 | 产生白色沉淀,反应方程式是:Na2CO3+CaCl2═2NaCl+CaCO3↓, 则猜想一不成立. | 第3组同学认为:此方 案还不能确定猜想二还是猜想三成立. |
| 第3组 |  | 滤液变红,则猜想三成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:第2组实验结束后,试管静置一段时间,取上层清液滴加酚酞溶液. |
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了如图两套装置进行实验:用胶头滴管吸取某种液体,锥形瓶中充入一种气体或
放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
(1)若甲中充入的气体是CO2,则可能发生反应的方程式CO2+2NaOH═Na2CO3+H2O.(任写一个)
(2)若乙中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是铁.(任写一种)
1.为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)检验氢氧化钙样品是否完全变质,进行如下实验,请将实验步骤和现象补充完整:
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数:
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.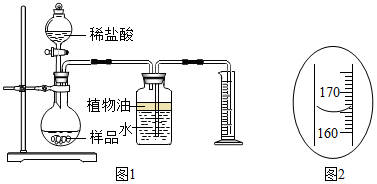
(2)实验中量筒的作用是收集排出的水,从而确定反应生成二氧化碳的体积.
(3)实验结束后,量筒内进入水的体积如图2所示.已知在该实验条件下,生成气体的密度为2克/升,通过计算,样品中R的质量分数为25%.
(4)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:稀盐酸进入烧瓶导致计算的二氧化碳体积偏大(写一个).
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)检验氢氧化钙样品是否完全变质,进行如下实验,请将实验步骤和现象补充完整:
| 实验步骤和现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,滴加酚酞试液,酚酞试液变红色 | 该样品还含有氢氧化钙 |
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(2)实验中量筒的作用是收集排出的水,从而确定反应生成二氧化碳的体积.
(3)实验结束后,量筒内进入水的体积如图2所示.已知在该实验条件下,生成气体的密度为2克/升,通过计算,样品中R的质量分数为25%.
(4)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:稀盐酸进入烧瓶导致计算的二氧化碳体积偏大(写一个).


