题目内容
元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息.
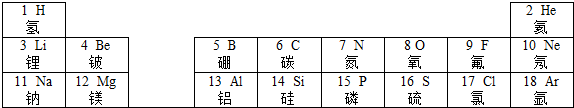
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是 ,该元素原子的质子数为 .
(2) 所表示的粒子符号为 ,它的最外层电子数为 .
所表示的粒子符号为 ,它的最外层电子数为 .
(3)由原子序数为8和13的两种元素组成的化合物是 (写化学式).
(4)如图表示气体分子示意模型,其中属于化合物的是 (填字母序号),属于混合物的是 (填字母序号).
选用元素周期表中元素,表示A图中的分子,化学式可能为 、 (写出两种即可).


请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是
(2)
 所表示的粒子符号为
所表示的粒子符号为(3)由原子序数为8和13的两种元素组成的化合物是
(4)如图表示气体分子示意模型,其中属于化合物的是
选用元素周期表中元素,表示A图中的分子,化学式可能为

考点:元素周期表的特点及其应用,纯净物和混合物的判别,单质和化合物的判别,原子结构示意图与离子结构示意图,化学式的书写及意义
专题:化学用语和质量守恒定律,物质的分类
分析:(1)根据地壳中各元素含量解答;
(2)根据原子结构示意图各部分含义解答;
(3)根据化合物化学式的写法解答;
(4)由多种物质组成的物质是混合物,由同种元素组成的纯净物是单质,由不同种元素组成的纯净物是化合物,利用该知识对问题进行分析即可.
(2)根据原子结构示意图各部分含义解答;
(3)根据化合物化学式的写法解答;
(4)由多种物质组成的物质是混合物,由同种元素组成的纯净物是单质,由不同种元素组成的纯净物是化合物,利用该知识对问题进行分析即可.
解答:解:(1)地壳中元素含量由高到低的顺序是氧硅铝铁,仅次于氧的非金属元素名称是硅,硅原子的质子数为14;
(2)图中粒子质子数为16,核外电子数为16,为硫原子,符号为S;最外层上有6个电子;
(3)原子序数为8和13的元素分别为氧和铝元素,两元素组成的化合物为氧化铝,已知铝元素的化合价为+3价,氧元素的化合价为-2价,利用化合价数值交叉法书写化学式,化学式为Al2O3,
(4)由图中可知,B中含有的分子种类是一种,且该分子是由不同原子构成,因此是由不同种元素组成的纯净物,属于化合物;C是含有两种不同的分子是由两种物质组成的物质,属于混合物;A图中的分子,一个分子是由两个原子构成的,所以可能是氢分子、氧分子(或氯分子),
故答案为:(1)硅、14;(2)S、6; (3)Al2O3;(4)H2,O2.
(2)图中粒子质子数为16,核外电子数为16,为硫原子,符号为S;最外层上有6个电子;
(3)原子序数为8和13的元素分别为氧和铝元素,两元素组成的化合物为氧化铝,已知铝元素的化合价为+3价,氧元素的化合价为-2价,利用化合价数值交叉法书写化学式,化学式为Al2O3,
(4)由图中可知,B中含有的分子种类是一种,且该分子是由不同原子构成,因此是由不同种元素组成的纯净物,属于化合物;C是含有两种不同的分子是由两种物质组成的物质,属于混合物;A图中的分子,一个分子是由两个原子构成的,所以可能是氢分子、氧分子(或氯分子),
故答案为:(1)硅、14;(2)S、6; (3)Al2O3;(4)H2,O2.
点评:本题难度不大,考查学生灵活运用元素周期表中元素的信息、化学式的书写等进行分析、解题的能力.

练习册系列答案
相关题目
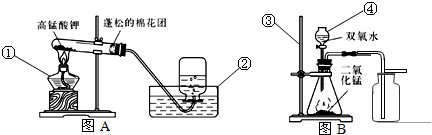

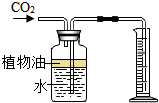 (1)课外实验活动中,某兴趣小组同学用加热碳酸氢钠(NaHCO3)固体(产物为Na2CO3、二氧化碳和水)来制取CO2,该反应的表达式为:
(1)课外实验活动中,某兴趣小组同学用加热碳酸氢钠(NaHCO3)固体(产物为Na2CO3、二氧化碳和水)来制取CO2,该反应的表达式为:
 关于电解水实验的叙述正确的是
关于电解水实验的叙述正确的是