题目内容
 (1)课外实验活动中,某兴趣小组同学用加热碳酸氢钠(NaHCO3)固体(产物为Na2CO3、二氧化碳和水)来制取CO2,该反应的表达式为:
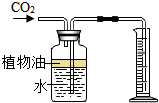
(1)课外实验活动中,某兴趣小组同学用加热碳酸氢钠(NaHCO3)固体(产物为Na2CO3、二氧化碳和水)来制取CO2,该反应的表达式为:(2)如图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是
(3)NaHCO3、Na2CO3、K2CO3 都能和稀盐酸发生类似于CaCO3与稀盐酸反应产生的CO2,要制得等质量CO2,消耗NaHCO3、Na2CO3、K2CO3、CaCO3质量最少的是
考点:盐的化学性质,量气装置,根据化学反应方程式的计算
专题:常见的盐 化学肥料
分析:(1)由题给条件直接写出碳酸钠分解的化学方程式,注意配平和气体符号的标注;
(2)二氧化碳能够溶于水,不溶于植物油,可以据此解答;
(3)根据碳元素的质量守恒来完成解答,结合这四种物质与盐酸反应的化学方程式可以知道二氧化碳中的碳元素和碳酸盐中的碳元素的质量相等,而即碳酸盐中碳元素的含量大,那么生成二氧化碳气体的质量就大,则需要的这种碳酸盐的质量就是最少的,可以据此解答该题.
(2)二氧化碳能够溶于水,不溶于植物油,可以据此解答;
(3)根据碳元素的质量守恒来完成解答,结合这四种物质与盐酸反应的化学方程式可以知道二氧化碳中的碳元素和碳酸盐中的碳元素的质量相等,而即碳酸盐中碳元素的含量大,那么生成二氧化碳气体的质量就大,则需要的这种碳酸盐的质量就是最少的,可以据此解答该题.
解答:解:(1)碳酸氢钠受热分解的化学方程式为:2NaHCO3
Na2CO3+H2O+CO2↑;
(2)量筒收集的水的体积,即为生成的二氧化碳的体积,在水面上放一层植物油的目的是防止二氧化碳溶于水;植物油上方原有的空气对实验结果无明显影响,因为植物油上方原有的空气不会进入量筒中.
(3)根据碳元素的质量守恒来完成解答,结合这四种物质与盐酸反应的化学方程式可以知道二氧化碳中的碳元素和碳酸盐中的碳元素的质量相等,而即碳酸盐中碳元素的含量大,那么生成二氧化碳气体的质量就大;设碳酸盐的质量为m,相对分子质量为M,则可以判断碳酸盐中碳元素的质量为:m×
,根据该计算式可以知道,当碳酸盐的质量相等时,该碳酸盐的相对分子质量越小生成的二氧化碳的质量越大,分析所给四种碳酸盐可以知道:M(NaHCO3)=84,M(Na2CO3)=106,M(K2CO3)=138,M(CaCO3)=100,所以可以判断生成二氧化碳气体的质量最大的为碳酸氢钠,那么若生成等质量的二氧化碳,需要的碳酸氢钠的质量也就是最小的.
故答案为:(1)2NaHCO3
Na2CO3+H2O+CO2↑;
(2)防止二氧化碳溶于水;无;
(3)NaHCO3.
| ||
(2)量筒收集的水的体积,即为生成的二氧化碳的体积,在水面上放一层植物油的目的是防止二氧化碳溶于水;植物油上方原有的空气对实验结果无明显影响,因为植物油上方原有的空气不会进入量筒中.
(3)根据碳元素的质量守恒来完成解答,结合这四种物质与盐酸反应的化学方程式可以知道二氧化碳中的碳元素和碳酸盐中的碳元素的质量相等,而即碳酸盐中碳元素的含量大,那么生成二氧化碳气体的质量就大;设碳酸盐的质量为m,相对分子质量为M,则可以判断碳酸盐中碳元素的质量为:m×
| 12 |
| M |
故答案为:(1)2NaHCO3
| ||
(2)防止二氧化碳溶于水;无;
(3)NaHCO3.
点评:本题综合考查了实验室制取二氧化碳的装置的选取、化学方程式的书写,书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.根据化学方程式的有关化学方程式的计算要细心、准确.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
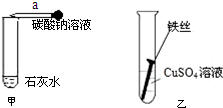 在某年的中考化学实验操作考试中,小红同学的考题是“盐的化学性质”.如图反映了小红操作的部分内容;
在某年的中考化学实验操作考试中,小红同学的考题是“盐的化学性质”.如图反映了小红操作的部分内容;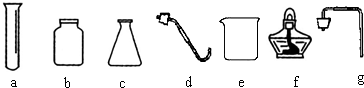
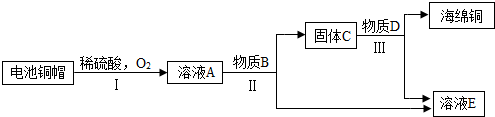
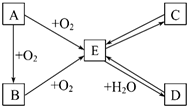 A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体,C为难溶于水的固体.其转化关系如图所示:
A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体,C为难溶于水的固体.其转化关系如图所示:
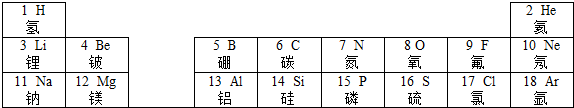
 所表示的粒子符号为
所表示的粒子符号为