题目内容
13.2003年12月23日,川东北气矿16H井发生硫化氢气体井喷事故,死亡243人.硫化氢是硫和氢的化合物,有毒性,一般用硫化亚铁和稀硫酸反应制取.…溶于水得氢硫酸,在空气中会被逐渐氧化,析出硫黄而浑浊.(1)请写出配制硫化氢的化学方程式:FeS+H2SO4=FeSO4+H2S↑
这个反应是非氧化还原反应(选填“氧化还原反应”或“非氧化还原反应”)
(2)硫化氢有毒,是它的化学性质(选填“物理性质”或“化学性质”);氢硫酸是混合物(选填“纯净物”或“混合物”)
(3)写出氢硫酸在空气中被氧化而析出硫黄的化学方程式:2H2S+O2=2S↓+2H2O,在这个反应中,O2是氧化剂.
(4)发生井喷后,为了缓解灾情,于是点燃了井喷的硫化氢气体,试写出化学方程式:2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+2SO2
(5)仿照氧化物的定义,与硫化氢同属一类的物质是①④⑤.
①甲烷 ②氢氧化钙 ③乙醇 ④氟化氢 ⑤水.
分析 (1)根据题意结合质量守恒定律来书写制取硫化氢的化学方程式;根据氧化还原反应的概念分析;
(2)根据化学性质的定义和物质分类分析;
(3)根据化学方程式的书写步骤分析;
(4)根据硫化氢在空气中完全燃烧的反应,写出反应的化学方程式;
(5)根据氢化物的概念进行分析.
解答 解:(1)硫化亚铁和稀硫酸反应后生成硫酸亚铁和硫化氢,故可以写出该反应的化学方程式;此反应中各元素的化合价在反应前后都没有改变,属于非氧化还原反应;
(2)硫化氢有毒需要在化学变化中表现出来,属于化学性质;氢硫酸是混合物;
(3)氢硫酸在空气中被氧化而析出硫黄的化学方程式是2H2S+O2=2H2O+2S↓;O2是氧化剂;
(4)硫化氢在空气中完全燃烧生成了二氧化硫和水,反应的化学方程式:2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O;
(5)氢化物即由两种元素组成,其中一种是氢元素的化合物,因此甲烷、氟化氢和水都是氢化物,氢氧化钙和乙醇都含有三种元素,不属于氢化物.
故答案为;(1)FeS+H2SO4=FeSO4+H2S↑;非氧化还原反应
(2)化学性质;混合物;
(3)2H2S+O2=2S↓+2H2O;O2
(4)2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+2SO2;
(5)①④⑤.
点评 本题主要考查化学方程式的书写、物质的分类等方面的知识,难度不大.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
3.某密闭容器内有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
下列说法正确的是C.
A.反应后X的质量为8g
B.Z与W的相对分子质量比一定是1:1
C.参加反应的X与Z的质量比是2:3
D.该反应属于置换或复分解反应(填反应类型)
| 物质 | X | Y | Z | W |
| 反应前质量/g | 4 | 1 | 10 | 2 |
| 反应后质量/g | 待测 | 5 | 4 | 8 |
A.反应后X的质量为8g
B.Z与W的相对分子质量比一定是1:1
C.参加反应的X与Z的质量比是2:3
D.该反应属于置换或复分解反应(填反应类型)
4.已知硝酸钾在20℃时的溶解度是31.6克,如果要改变硝酸钾的溶解度,可行的是( )
| A. | 改变溶剂的量 | B. | 改变温度 | ||
| C. | 改变搅拌的速度 | D. | 改变硝酸钾的颗粒大小 |
8.某则广告中说:“吃完饭后,口中的酸碱度会降低”,这里“降低”的指的是( )
| A. | pH上升 | B. | pH=7 | C. | pH向7靠拢 | D. | pH降低 |
3.下列俗语与物质化学性质无关的是( )
| A. | 玉不琢不成器 | B. | 火上加油 | C. | 百炼成钢 | D. | 死灰复燃 |
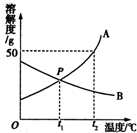 图是A、B两种固体物质的溶解度曲线.
图是A、B两种固体物质的溶解度曲线. 锌是人体健康必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫功能低下.如图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:
锌是人体健康必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫功能低下.如图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答: