题目内容
16.固体氢氧化钠放置在空气中容易变质转化为碳酸钠(假设不含其它杂质).某化学兴趣小组为了测定故置于空气中的氢氧化钠的变质程度.他们用氢氧化钠样品和稀盐酸完成了如图实验.试计算:
(1)恰好完全反应时,产生气体的质量是2.2g
(2)样品中氢氧化钠的质量分数是多少?(精确到0.1%)
分析 (1)根据质量守恒定律分析产生气体的质量;
(2)根据碳酸钠能与盐酸反应生成了二氧化碳,由二氧化碳的质量求出碳酸钠的质量,再求出氢氧化钠的质量,即可求出样品中氢氧化钠的质量分数.
解答 解:(1)根据质量守恒定律,产生气体的质量200g+17.3g-215.1g=2.2g;故填:2.2;
(2)样品中碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
样品中氢氧化钠的质量分数是=$\frac{17.3g-5.3g}{17.3g}×$100%=69.4%
答:该样品中氢氧化钠的质量分数为69.4%.
点评 此题是对化学方程式以及溶液相关问题的考查,利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.

练习册系列答案
相关题目
6.下列“家庭小实验”中,不能达到预期目的是( )
| A. | 用某些植物的花瓣制酸碱指示剂 | |
| B. | 用碎鸡蛋壳和食盐水制二氧化碳 | |
| C. | 用柠檬酸、果汁、白糖、水、小苏打等自制汽水 | |
| D. | 用石子、细沙、活性炭、棉、纱布等制作简易净水器 |
7.下列物质加入水中能形成溶液的是( )
| A. | 粉笔灰 | B. | 冰块 | C. | 生铁 | D. | 蔗糖 |
4.放入水中不能形成溶液的物质是( )
| A. | 面粉 | B. | 白酒 | C. | 白糖 | D. | 食盐 |
11.金属钯(Pd)是种用于制首饰的银白色贵金属,现进行如下三个实验:
由上述现象可知,钯在金属活动性顺序中位于( )
| 实验一 | 实验二 | 实验三 | |
| 实验操作 | 将钯丝伸入稀盐酸 | 将银丝伸入PdCl2溶液 | 将铂丝伸入PdCl2溶液 |
| 实验现象 | 无明显现象 | 银丝表面析出固体 溶液中出现白色沉淀 | 无明显现象 |
| A. | 氢之前 | B. | 银和铂之间 | C. | 氢和银之间 | D. | 铂之后 |
1.2017年2月8日晚铜陵化工厂爆炸事故再次给我们敲响了安全警钟.化学实验中的先后顺序不但影晌着实验成败与否,还可能造成身体伤害.下列实验顺序正确的是( )
| A. | 稀释浓硫酸时,先倒浓硫酸再慢慢倒入水并不断搅拌 | |
| B. | 氢氧化钠溶液溅到皮肤上,先涂硼酸溶液再用水冲洗 | |
| C. | 检查装置气密性时,先将导管插入水中再给装置加热 | |
| D. | 排水法收集气体,先熄灭酒精灯再将导气管移出水槽 |
8.合肥郊区的农民将农作物秸秆粉碎后放在密闭的沼气池内发酵制沼气,发酵后的残余物可作肥料,沼气是一种清洁燃料,其主要成分是甲烷(CH4).化学小组的同学围绕“秸秆主要由哪些元素组成”这一问题展开了以下探究活动.
【猜想与假设】秸秆中一定含有碳元素、氢元素和氧元素.
【结论与解释】依据化学反应前后元素的种类不变,同学们得出秸秆中含有C、H、O三种元素的结论.
【反思与评价】你认为同学们得出的结论是否正确并说明理由:不正确,因为氧气参加了反应,因此无法确定秸秆中是否含有氧元素.
【拓展与应用】农村传统的处理秸秆方式是直接烧掉,试从环境、原料利用等方面说明将农作物秸秆制成沼气的重要意义是:节约资源,更环保.写出甲烷在足量氧气中燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
【猜想与假设】秸秆中一定含有碳元素、氢元素和氧元素.
| 探究步骤 | 实验现象 | 相关结论 |
| 用坩埚钳夹持一小段干燥的秸秆,点燃后伸入盛有氧气的集气瓶中 | 秸秆剧烈燃烧,火焰熄灭后观察到瓶壁出现水珠 | 产物中有H2O |
| 再向集气瓶中滴入少量澄清石灰水 | 观察到有白色沉淀物 | 产物中有CO2 |
【反思与评价】你认为同学们得出的结论是否正确并说明理由:不正确,因为氧气参加了反应,因此无法确定秸秆中是否含有氧元素.
【拓展与应用】农村传统的处理秸秆方式是直接烧掉,试从环境、原料利用等方面说明将农作物秸秆制成沼气的重要意义是:节约资源,更环保.写出甲烷在足量氧气中燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
5. 小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
【实验反思】小红经过分析认为1号溶液还可能是变质的氢氧化钠溶液,写出氢氧化钠溶液变质的化学方程式2NaOH+CO2═Na2CO3+H2O.
 小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
| 实验步骤 | 实验现象 | 实验结论 |
实验1:分别测定两种溶液的pH 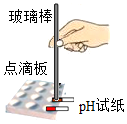 | 两种溶液的pH均大于7 | 两瓶溶液一定不是NaCl溶液、Na2SO4溶液 |
实验2: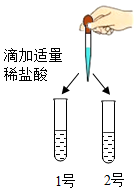 | 均有气泡产生 | 两瓶溶液分别是NaHCO3溶液和Na2CO3溶液.写出Na2CO3溶液与盐酸反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑. |
实验3:滴加适量氯化钙溶液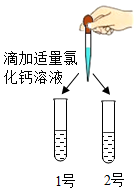 | 1号试管中出现白色沉淀,2号试管中无明显现象 | 1号溶液是Na2CO3溶液 2号溶液是NaHCO3溶液. |
 表示氢原子 用
表示氢原子 用 表示氧原子,下列模型能表示变成了水蒸汽的这部分水分子的是( )
表示氧原子,下列模型能表示变成了水蒸汽的这部分水分子的是( )


