题目内容
7.推理是化学学习中常用的思维方法. 以下推理正确的是CA.原子在化学变化中不能再分,所以分子在化学变化中也不能再分
B.单质中只含一种元素,所以只含一种元素的物质一定是单质.
C.燃烧需要同时满足三个条件,所以破坏其中一个条件就可以灭火
D.蜡烛燃烧生成 CO2和 H2O,所以蜡烛组成里一定含有C和H.
分析 根据已有的知识进行分析,原子在化学变化中不能再分,分子可以再分,臭氧和氧的混合物中只含氧这一种元素,但它是混合物,所以不是单质,燃烧需要同时满足三个条件,灭火只要破坏其中的一个条件即可,根据质量守恒定律的元素守恒进行解答.
解答 解:A、在化学变化中分子可以再分,原子不可以再分,故A错误;
B、含一种元素的物质不一定是单质,如臭氧和氧的混合物中只含氧这一种元素,但它是混合物,所以不是单质,故B错误;
C、燃烧需要同时满足三个条件,灭火只要破坏其中的一个条件即可,故正确;
D、根据质量守恒定律的元素守恒,因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H;
故选:C;C和H;
点评 本题考查了关于化学知识的总结,完成此题,可以依据已有的化学知识进行,要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列物质排放到空气中,不会造成大气污染的是( )
| A. | 二氧化硫 | B. | 一氧化碳 | C. | 氮气 | D. | 氮氧化合物 |
18.将一定量的铁粉投入硫酸铜溶液中,充分反应后,铁粉有剩余,则所得溶液中的溶质是( )
| A. | 硫酸铁 | B. | 硫酸亚铁 | ||
| C. | 硫酸铁和硫酸铜 | D. | 硫酸亚铁和硫酸铜 |
15.有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成,为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,BaSO4不溶于酸,经过思考设计了以下实验.请分析实验过程,回答下列问题:

(1)白色粉末中一定不含CuSO4、Na2SO4;可能含有NaOH.
(2)生成白色沉淀的化学方程式为Na2CO3+CaCl2═2NaCl2+CaCO3↓.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】
猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
【进行实验】
【得出结论】白色粉末的成分是Na2CO3、BaCl2、NaOH.

(1)白色粉末中一定不含CuSO4、Na2SO4;可能含有NaOH.
(2)生成白色沉淀的化学方程式为Na2CO3+CaCl2═2NaCl2+CaCO3↓.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】
猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取无色滤液少许于试管中,滴加过量的BaCl2溶液 | 产生白色沉淀 | 猜想Ⅱ不成立 |
| ②在①反应后的试管中滴加无色酚酞溶液 | 溶液变为红色 | 猜想Ⅲ成立 |
2. 工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
提出假设:
假设一:滤液中只含氢氧化钠
假设二:滤液中含氢氧化钠和氢氧化钙
假设三:滤液中含氢氧化钠和碳酸钠
假设四:滤液中含氢氧化钠、氢氧化钙和碳酸钠
甲同学设计了如表实验方案:
已知:Na2CO3+CaCl2═2NaCl+CaCO3↓(白色),试回答:
(1)写出碳酸钠溶液与石灰水反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)哪种假设不合理,试说明理由假设四不合理,因为氢氧化钙溶液与碳酸钠溶液不能共存.
(3)乙同学认为甲同学设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,她的理由是若氢氧化钙过量与氯化钙不发生反应.
(4)丙同学认为要说明碳酸钠溶液与石灰水是否恰好完全反应,还需在甲同学实验方案的基础上增加一个实验.她的实验方案是:
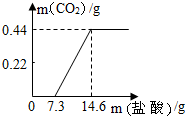
(5)取18.6g氢氧化钠样品(样品中的杂质是碳酸钠),加水溶解得到溶液A,取A溶液的$\frac{1}{10}$向其中逐滴加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗盐酸的质量(所得数据如图).请完成下列任务:
①写出如图中ab段发生反应的化学方程式NaOH+HCl═NaCl+H2O.
②样品中碳元素的质量分数为6.5%.(结果保留到0.1%)
 工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.提出假设:
假设一:滤液中只含氢氧化钠
假设二:滤液中含氢氧化钠和氢氧化钙
假设三:滤液中含氢氧化钠和碳酸钠
假设四:滤液中含氢氧化钠、氢氧化钙和碳酸钠
甲同学设计了如表实验方案:
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液放在试管中,再滴入氯化钙溶液 | 若生成白色沉淀 | 碳酸钠过量 |
| 若无明显现象 | 恰好反应 |
(1)写出碳酸钠溶液与石灰水反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)哪种假设不合理,试说明理由假设四不合理,因为氢氧化钙溶液与碳酸钠溶液不能共存.
(3)乙同学认为甲同学设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,她的理由是若氢氧化钙过量与氯化钙不发生反应.
(4)丙同学认为要说明碳酸钠溶液与石灰水是否恰好完全反应,还需在甲同学实验方案的基础上增加一个实验.她的实验方案是:
| 实验步骤 | 实验现象和结论 |
①写出如图中ab段发生反应的化学方程式NaOH+HCl═NaCl+H2O.
②样品中碳元素的质量分数为6.5%.(结果保留到0.1%)
19.有关水的认识正确的是( )
| A. | 电解水得到H2和O2,说明水是由氢元素和氧元素组成的 | |
| B. | 利用沉淀、过滤、吸附、电解等方法可以净化水 | |
| C. | 生活中用过滤的方法可以降低水的硬度 | |
| D. | 物质溶于水所得到的溶液是均一、稳定、无色、透明的 |
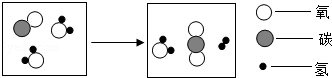 如图表示在一定条件下,物质转化过程的微观示意图,请根据图形信息回答问题:
如图表示在一定条件下,物质转化过程的微观示意图,请根据图形信息回答问题: