题目内容
已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)
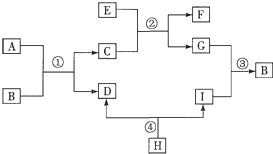
(1)E的名称是 ,B,C,H 的化学式分别是 , , .
(2)写出反应①的化学方程式: .
(3)写出反应②的化学方程式: .
(4)写出反应③的化学方程式: .

(1)E的名称是
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
(4)写出反应③的化学方程式:
考点:物质的鉴别、推断,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:做推断题的关键是找突破口,突破口一般是颜色和重要的化学反应等.G为“紫红色金属”,为铜.而“E为目前世界上产量最高的金属”,为铁.“I是地壳中含量最高的元素形成的常见气体单质”,所以为氧气.“A在人体胃液中可以帮助消化”,所以为盐酸.
解答:解:根据题意:G为“紫红色金属”,为铜.而“E为目前世界上产量最高的金属”,为铁.“I是地壳中含量最高的元素形成的常见气体单质”,所以为氧气.A“在人体胃液中可以帮助消化”,所以为盐酸.由于铜(G)可以和氧气(I)反应生成B,所以B为氧化铜.则A和B反应生成C和D为盐酸和氧化铜反应生成水和氯化铜,而C能够和铁反应,所以C为氯化铜,D为水.H能够生成水和氧气,所以H为过氧化氢.而EC反应即为铁与氯化铜的反应生成氯化亚铁(F)和铜(G).
所以转化关系为:
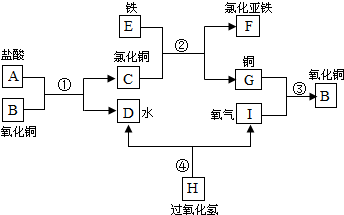
根据图框,则各反应的化学方程式为:
①CuO+2HCl=CuCl2+H2O,为复分解反应;
②Fe+CuCl2=FeCl2+Cu,为置换反应;
③2Cu+O2
2CuO,为化合反应;
④2H2O2
2H2O+O2↑,为分解反应.
故答案为:
(1)铁,CuO,CuCl2,H2O2.
(2)CuO+2HCl=CuCl2+H2O.
(3)Fe+CuCl2=FeCl2+Cu.
(4)2Cu+O2
2CuO.
所以转化关系为:

根据图框,则各反应的化学方程式为:
①CuO+2HCl=CuCl2+H2O,为复分解反应;
②Fe+CuCl2=FeCl2+Cu,为置换反应;
③2Cu+O2
| ||
④2H2O2
| ||
故答案为:
(1)铁,CuO,CuCl2,H2O2.
(2)CuO+2HCl=CuCl2+H2O.
(3)Fe+CuCl2=FeCl2+Cu.
(4)2Cu+O2
| ||
点评:掌握推断题的做题方法,首先寻找突破口,突破口一般是颜色和重要的化学反应等,同时要敢于尝试.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目



 某班同学做常见酸和碱与酚酞反应的实验,本次实验后废液分别集中到一个废液缸中.负责清洁实验室的小雪、小丽、小明和小华四位同学围绕如何处理“废液”展开了讨论:
某班同学做常见酸和碱与酚酞反应的实验,本次实验后废液分别集中到一个废液缸中.负责清洁实验室的小雪、小丽、小明和小华四位同学围绕如何处理“废液”展开了讨论: 如图所示,物质王国的“小朋友”们手拉手围成一圈做游戏.
如图所示,物质王国的“小朋友”们手拉手围成一圈做游戏. 指出如图中的错误操作
指出如图中的错误操作