题目内容
8.向盛有Fe(NO3)2、AgNO3的溶液中加入一定量的Zn粉,充分反应后过滤,得到滤渣和无色滤液两部分:(1)滤渣中一定含有的金属是Ag、Fe;
(2)请写出Zn粉与AgNO3溶液反应的化学方程式Zn+2AgNO3=Zn(NO3)2+2Ag.
分析 锌比铁活泼,铁比银活泼,向盛有Fe(NO3)2、AgNO3的溶液中加入一定量的Zn粉,锌先和硝酸银反应,硝酸银完全反应后如果锌有剩余,则锌再和硝酸亚铁反应.
解答 解:(1)向盛有Fe(NO3)2、AgNO3的溶液中加入一定量的Zn粉,锌先和硝酸银反应,硝酸银完全反应后如果锌有剩余,则锌再和硝酸亚铁反应,充分反应后过滤,得到无色滤液,说明硝酸银和硝酸亚铁都已经完全反应,滤渣中一定含有的金属是反应生成的Ag、Fe.
故填:Ag、Fe.
(2)Zn粉与AgNO3溶液反应生成硝酸锌和银,反应的化学方程式为:Zn+2AgNO3=Zn(NO3)2+2Ag.
故填:Zn+2AgNO3=Zn(NO3)2+2Ag.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
19.下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
| A. | 铁和稀硫酸 | B. | 氢氧化钾溶液中加入稀硝酸 | ||
| C. | 硫酸铜溶液中加入锌片 | D. | 氢氧化钙溶液中加入碳酸钾溶液 |
13.下列事实和相应的解释不正确的是( )
| A. | 导致甲状腺肿大的原因--可能是因为缺乏碘元素 | |
| B. | 反应前后质量守恒--反应前后原子的质量和数目不变 | |
| C. | 乐事薯片用氮气包装--氮气的化学性质不活泼 | |
| D. | 空气可以被压缩--分子在不断运动 |
20.下列属于纯净物的是( )
| A. | 大理石 | B. | 五氧化二磷 | C. | 加碘食盐 | D. | 食醋 |
17.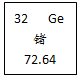 锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )
锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )
 锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )
锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )| A. | 原子序数为32 | B. | 元素名称为锗 | ||
| C. | 元素符号为Ge | D. | 相对原子质量为32 |