题目内容
17.过氧化氢溶液生成氧气的快慢与什么因素有关”的课题进行探险究,以下是他研究性学习小组选择们探究的主要过程:【假设】过氧化氢溶液生成氧气的快慢与催化剂的种类有关.
【实验方案】常温下,在两瓶相同体积的过氧化氢溶液中分别加入相同质量的二氧化锰和红砖粉,测量各生成一瓶(相同体积)氧气所需要的时间.
【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 6% 过氧化氢溶液 | 6% 过氧化氢溶液 |
| 催化剂 | 1g红砖粉 | 1g 二氧化锰 |
| 时间 | 152s | 35s |
【反思】过氧化氢溶液在常温下分解缓慢,分别放入二氧化锰或红砖粉后反应明显加快,若要证明二氧化锰和红砖粉是该反应的催化剂,还需要增加实验证明它们在化学反应前后的质量、化学性质是否改变.过氧化氢溶液生成氧气的快慢还与哪些因素有关?请说出你的一个猜想:H2O2生成O2的快慢与H2O2的质量分数有关(合理即可).
【实验方案】在温度、相同质量的相同催化剂的条件下,采用等质量但不同的浓度的过氧化氢溶液来进行实验,然后测量收集相同体积的气体所需的时间,从而得出结论.故填:在温度、相同质量的相同催化剂的条件下,采用等质量但不同的浓度的过氧化氢溶液来进行实验,然后测量收集相同体积的气体所需的时间.
分析 【实验结论】根据表中提供的数据可以进行相关方面的判断;
【反 思】根据催化剂的定义进行反思;
【假 设】可以联系反应物的浓度对反应速率的影响,利用控制变量法来进行设计实验.
【实验方案】根据作出的假设采用控制变量法来进行设计实验进行验证.
解答 解:【实验结论】根据控制变量法,分析表中的有关数据,可知分别用1g红砖粉和1gMnO2做催化剂,来催化反应时所用的时间分别是165s和46s;由此可知,用1gMnO2做催化剂要比用1g红砖粉做催化剂时,化学反应速率要快.因此,由实验现象可以得出的实验结论是:H2O2生成氧气的快慢与催化剂种类有关.故填:相同条件下H2O2生成O2的快慢与催化剂的种类有关;
【反思】根据催化剂的概念可知,催化剂能改变化学反应的速率,而本身的质量和化学性质在反应前后不改变.故填:质量;化学性质;
【假设】可以假设:H2O2生成氧气的快慢与过氧化氢的浓度有关.故填:H2O2生成O2的快慢与H2O2的质量分数有关(合理即可);
【实验方案】在温度、相同质量的相同催化剂的条件下,采用等质量但不同的浓度的过氧化氢溶液来进行实验,然后测量收集相同体积的气体所需的时间,从而得出结论.故填:在温度、相同质量的相同催化剂的条件下,采用等质量但不同的浓度的过氧化氢溶液来进行实验,然后测量收集相同体积的气体所需的时间.
点评 本题主要考查了催化剂的催化作用及其正确设计实验方案等方面的内容.可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
1.如图所示曲线能正确表达对应的反应或过程的是( )
| A. |  碳在盛有空气的密闭容器内燃烧 | |
| B. |  铁在装有氧气的密闭容器中燃烧 | |
| C. |  向一定量的二氧化锰中加入过氧化氢中 | |
| D. |  将水通电一段时间 |
5. 小明发现二氧化锰催化 过氧化氢分解的实验中,反应速度逐渐变慢.查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低.为了探究二氧化锰催化能力降低的影响因素,进行如下实验.
小明发现二氧化锰催化 过氧化氢分解的实验中,反应速度逐渐变慢.查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低.为了探究二氧化锰催化能力降低的影响因素,进行如下实验.
【材料准备】取三份质量均为2锰分别催化40毫升溶质质量分数为10%、20%、30%的过氧化氢溶液分解,实验后回收二氧化锰,并分别标为A、B、C;另取多次催化分解10%过氧化氢溶液实验后回收的二氧化锰,标为D.
【实验步骤】①连接实验装置并检查气密性.
②取未使用过的二氧化锰0.5克,加入锥形瓶中,再加入10毫升溶质质量分数为5%的过氧化氢溶液,记录收集120毫升氧气所需的时间.
③再分别取A、B、C、D组二氧化锰各0.5克,重复上述实验.
④多次实验取平均值,记录数据如下:
(1)实验时,长颈漏斗下端管口在应液面以下,其目的是防止产生的气体从长颈漏斗中逸出.
(2)实验中,通过比较收集相同体积氧气所需的时间外,还可以通过比较相同时间内产生气体的体积来反映二氧化锰的催化能力.
(3)由上表数据可知,引起回收的二氧化锰催化能力下降的因素是过氧化氢溶液的溶质质量分数、二氧化锰使用的次数.
 小明发现二氧化锰催化 过氧化氢分解的实验中,反应速度逐渐变慢.查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低.为了探究二氧化锰催化能力降低的影响因素,进行如下实验.
小明发现二氧化锰催化 过氧化氢分解的实验中,反应速度逐渐变慢.查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低.为了探究二氧化锰催化能力降低的影响因素,进行如下实验.【材料准备】取三份质量均为2锰分别催化40毫升溶质质量分数为10%、20%、30%的过氧化氢溶液分解,实验后回收二氧化锰,并分别标为A、B、C;另取多次催化分解10%过氧化氢溶液实验后回收的二氧化锰,标为D.
【实验步骤】①连接实验装置并检查气密性.
②取未使用过的二氧化锰0.5克,加入锥形瓶中,再加入10毫升溶质质量分数为5%的过氧化氢溶液,记录收集120毫升氧气所需的时间.
③再分别取A、B、C、D组二氧化锰各0.5克,重复上述实验.
④多次实验取平均值,记录数据如下:
| 组别 | 未使用过的二氧化锰 | A | B | C | D |
| 收集氧气时间/秒 | 17.9 | 23.2 | 27.7 | 32.3 | 37.8 |
(2)实验中,通过比较收集相同体积氧气所需的时间外,还可以通过比较相同时间内产生气体的体积来反映二氧化锰的催化能力.
(3)由上表数据可知,引起回收的二氧化锰催化能力下降的因素是过氧化氢溶液的溶质质量分数、二氧化锰使用的次数.
7.下列图示的实验中涉及到化学变化的是( )
| A. | 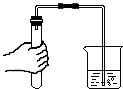 检查装置的气密性 | B. | 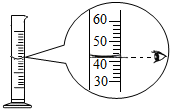 读取水的体积 | ||
| C. | 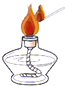 点燃酒精灯 | D. |  活性炭吸附红棕色二氧化氮 |


