题目内容
17.分别用两种方法测定10g铜锌合金中锌的含量.| 加入的试剂 | 测的数据 | |
| 方法1 | 足量稀硫酸 | 气体0.2g |
| 方法2 | 足量硫酸铜溶液 | 固体质量减少0.1g |
分析 方法一:根据氢气的质量计算锌的质量,进一步计算Cu-Zn合金粉中锌的质量分数;
方法二:根据质量差法计算分析.
解答 解:方法一:设Cu-Zn合金粉中锌的质量为x.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
$\frac{65}{x}=\frac{2}{0.2g}$
x=6.5g
Cu-Zn合金粉中锌的质量分数$\frac{6.5g}{20g}$×100%=32.5%;
方法二:Cu-Zn合金粉中锌的质量为x.
Zn+CuSO4═ZnSO4+Cu固体质量增加
65 64 65-64=1
x 0.1 g
$\frac{65}{x}=\frac{1}{0.1g}$
x=6.5 g
Cu-Zn合金粉中锌的质量分数$\frac{6.5g}{20g}$×100%=32.5%;
答:Cu-Zn合金粉中锌的质量分数32.5%.
点评 本题主要考查学生对金属的化学性质的认识,以及运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
7.将A、B、C三种物质放入密闭容器中,在一定条件下充分反应后(生成一定质量的D),测得反应物和产物在反应前后的质量如表所示:
对该反应的下列说法错误的是( )
| 物质 | A | B | C | D |
| 反应前(g) | 17 | 16 | 15 | 0 |
| 反应后(g) | 13 | X | 26 | Y |
| A. | 该项反应的A、B的质量比为1:1 | |
| B. | 该反应中X的值是16 | |
| C. | 该反应中Y的值是9 | |
| D. | 若A、B、C、D的相对分子质量分别为16、32、44、18,则该反应的化学方程式可表示为A+B=C+D |
8.下列关于物质的性质和用途说法不正确的是( )
| A. | 氧气用于火箭发射,是利用氧气的可燃性 | |
| B. | 氮气用来保护粮食,是利用氮气常温下化学性质稳定 | |
| C. | 稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光 | |
| D. | 二氧化碳用于灭火,是利用它的物理性质和化学性质 |
9.下列物质的用途不是利用其化学性质的是( )
| A. | 液态氨做制冷剂 | B. | 用O2炼钢 | ||
| C. | 氢气做清洁高效的新能源 | D. | 焦炭用于炼铁 |
7.过氧化钠(Na2O2)是潜水艇中氧气的再生剂,有关过氧化钠说法正确的是( )
| A. | 摩尔质量为78 | |
| B. | 0.5mol Na2O2中含16克氧元素 | |
| C. | 过氧化钠由二个钠原子和一个氧分子构成 | |
| D. | 该物质中两种元素的质量比为1:1 |
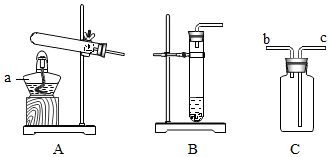 实验小组进行了如下实验.
实验小组进行了如下实验.
