题目内容
19. 学习酸碱中和反应时,很多同学对其产生探究兴趣.
学习酸碱中和反应时,很多同学对其产生探究兴趣.(1)甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论.乙同学认为甲同学推理不合理,理由是氢氧化钠固体溶于水放热.
(2)配制40g10%的氢氧化钠溶液.
步骤为:计算、称量、量取、溶解、装瓶并贴标签.量取水时如俯视读数,则配得的溶液溶质质量分数将大于(填“大于”、“小于”或“等于”)10%,最后将氢氧化钠溶液转移到试剂瓶中,贴上标签备用,在标签上应注明的是BC(填字母).
A.40gB.10%C.NaOH溶液
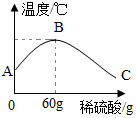
(3)乙同学为了验证甲同学的结论,将实验加以改进:将稀硫酸慢慢入装有40g10%氢氧化钠溶液的烧杯中,用温度计测出反应后液温度随加入稀硫酸质量的变化如图所示:
①B到C的过程中,烧杯内溶液中含有的阳离子有Na+、H+(填离子符号).
②恰好完全反应时所得溶液中溶质质量分数?7.1%(写出计算过程)
分析 (1)根据氢氧化钠溶于水放出大量的热进行分析;
(2)根据配制一定质量分数溶液的步骤是:计算、称量、量取、溶解、装瓶,量取水时如俯视读数,量取水的体积偏小,标签上应注明的是溶液的浓度和溶液名称进行分析;
(3)根据B点的温度最高,说明氢氧化钠和硫酸在B点恰好完全反应进行分析;
根据氢氧化钠和硫酸反应生成硫酸钠和水,依据题中的数据减小计算.
解答 解:(1)氢氧化钠固体溶于水会放出大量的热,因此使用氢氧化钠固体和稀硫酸反应放热不能得出中和反应放热的结论;
(2)配制一定质量分数溶液的步骤是:计算、称量、量取、溶解、装瓶,量取水时如俯视读数,量取水的体积偏小,所以配得的溶液溶质质量分数将大于10%,标签上应注明的是溶液的浓度和溶液名称,故选:BC;
(3)B→C,硫酸过滤,此时溶液中的溶质硫酸钠和稀硫酸,故烧杯内溶液中含有的阳离子有钠离子和氢离子;
设生成硫酸钠的质量为y,
H2SO4 +2NaOH=2H2O+Na2SO4
80 142
40g×10% y
$\frac{80}{40g×10%}$=$\frac{142}{y}$
y=7.1g
反应后所得溶液中溶质的质量分数Na2SO4%=$\frac{7.1g}{60g+40g}$×100%=7.1%.
故答案为:(1)氢氧化钠固体溶于水放热;
(2)计算,大于,BC;
(3)Na+、H+;7.1%.
点评 本题主要考查学生运用化学方程式进行计算的能力,掌握相关的溶液及化学方程式基本计算是解题的关键所在.

练习册系列答案
相关题目
10.小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”.测得实验数据如下:某金属与同体积盐酸溶液反应实验数据
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素盐酸溶液浓度、反应时溶液温度.
(2)可以通过比较反应开始到2分钟产生的气体体积实验数据来确定金属和酸反应的快慢.
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢.可能的原因是温度对反应速率的影响大于盐酸溶液浓度对反应速率的影响.
| 盐酸溶液浓度 | 5% | 10% | 15% | 5% | 10% | 15% |
| 反应开始时酸溶液的温度(℃) | 20 | 20 | 20 | 35 | 35 | 35 |
| 反应开始到2分钟产生的气体体积(mL) | 10 | 19 | 28 | 28 | 72 | 103 |
| 反应结束共产生气体体积(mL) | 60 | 118 | 175 | 60 | 118 | 175 |
(2)可以通过比较反应开始到2分钟产生的气体体积实验数据来确定金属和酸反应的快慢.
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢.可能的原因是温度对反应速率的影响大于盐酸溶液浓度对反应速率的影响.
7.碳在氧气中燃烧,下列说法符合质量守恒定律的是( )
| A. | 10g碳与12g氧气充分反应,可生成22g二氧化碳 | |
| B. | 32g碳与12g氧气充分反应,可生成44g二氧化碳 | |
| C. | 6g碳与16g氧气充分反应,可生成22g二氧化碳 | |
| D. | 8g碳与3g氧气充分反应,可生成11g二氧化碳 |
11.实验室制取氧气、氢气和二氧化碳的反应原理,从基本反应类型来看,不包含( )
| A. | 复分解反应 | B. | 置换反应 | C. | 化合反应 | D. | 分解反应 |
8.下列微粒属于阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |
9.下列应用和相应的原理(用化学方程式表示)及对应的基本反应类型均正确的是( )
| A. | 铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$F e3O4 氧化反应 | |
| B. | 比较铜和银的活动性:Cu+2AgCl═CuCl2+2Ag 置换反应 | |
| C. | 用过氧化氢溶液制取氧气:2H2O2 $\frac{\underline{\;红砖粉末\;}}{\;}$2H2O+O2分解反应 | |
| D. | 用盐酸除水垢的一个反应:Mg(OH)2+2HCl=MgCl2+H2O 复分解反应 |
 如图是有关氧气的知识网络图(反应条件部分省略),用化学用语填空:
如图是有关氧气的知识网络图(反应条件部分省略),用化学用语填空: