题目内容
6g大理石样品与50g稀盐酸恰好完全反应(杂质不参与反应且不溶于水),生成二氧化碳2.2g。求:反应后溶液中溶质的质量分数(计算结果保留一位小数)。
【答案】
【解析】
试题分析:反应后溶液中溶质的质量分数等于溶质的质量除以溶液的质量,反应后的溶质是氯化钙,可通过化学方程式求出;溶液的质量等于加入的物质的质量减去气体的质量;
解:设生成的CaCl2的质量为x,反应的CaCO3的质量为y 。
CaCO3+ 2HCl = CaCl2 + CO2 +H2O
100 111 44
y x 2.2g
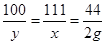
x=5.55g y=5g
CaCl2溶液的质量分数为: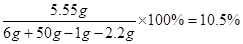
答:所得CaCl2溶液的质量分数为10.5%。
考点:有关溶质质量分数的计算

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
我市有丰富的大理石资源,大理石的主要成分是碳酸钙.小军同学在课余时间采集了一种大理石样品,为了测定这种大理石样品中碳酸钙的质量分数,他进行了如下四步实验:
| 实验步骤 | ①称烧杯的质量 | ②将适量稀盐酸加入烧杯中并称重 | ③称取少量大理石样品,并加入②的烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验数据 | 烧杯的质量为50.0g | 烧杯和稀盐酸的质量为l00.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
(1)实验过程中生成的二氧化碳质量是多少?
(2)这种大理石样品中碳酸钙的质量分数是多少?【假设稀盐酸只与样品中的碳酸钙反应,其反应原理:CaCO3+2HCl═CaCl2+H2O+CO2↑】
我市有丰富的大理石资源,大理石的主要成分是碳酸钙.小军同学在课余时间采集了一种大理石样品,为了测定这种大理石样品中碳酸钙的质量分数,他进行了如下四步实验:
请你计算:
(1)实验过程中生成的二氧化碳质量是多少?
(2)这种大理石样品中碳酸钙的质量分数是多少?【假设稀盐酸只与样品中的碳酸钙反应,其反应原理:CaCO3+2HCl═CaCl2+H2O+CO2↑】
| 实验步骤 | ①称烧杯的质量 | ②将适量稀盐酸加入烧杯中并称重 | ③称取少量大理石样品,并加入②的烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验数据 | 烧杯的质量为50.0g | 烧杯和稀盐酸的质量为l00.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
(1)实验过程中生成的二氧化碳质量是多少?
(2)这种大理石样品中碳酸钙的质量分数是多少?【假设稀盐酸只与样品中的碳酸钙反应,其反应原理:CaCO3+2HCl═CaCl2+H2O+CO2↑】