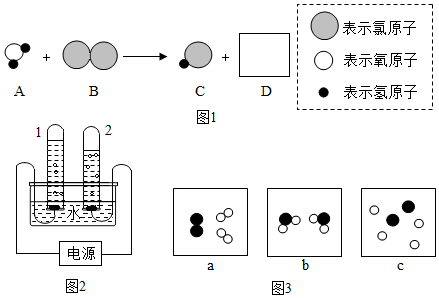
题目内容
2.钢铁工业是国家工业的基础.(1)如图甲是炼铁高炉及炉内化学变化过程示意图,根据图示回答有关问题.
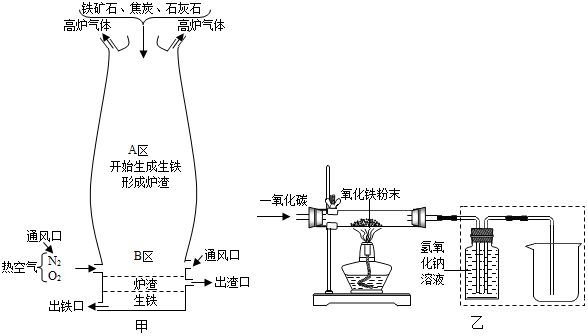
若图甲中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;点燃\;}}{\;}$2CO.
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如图乙.
【进行实验】该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g).
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量).
【分析与讨论】本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中同体产物可能有四氧化三铁、氧化亚铁、铁.
③铁及部分铁的氧化物的相关物理性质如表所示.
 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
①该小组同学将反应后的黑色同体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色同体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁b.四氧化三铁 c.四氧化三铁和铁
【得出结论】通过利用实验中获得的数据进行计算,得出黑色固体粉末为四氧化三铁(填名称).
【反思与评价】
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有AB.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
分析 (1)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
碳燃烧生成二氧化碳,二氧化碳在高温条件下和碳反应生成一氧化碳;
(2)为了防止发生爆炸,加热前应该先通入一会儿一氧化碳,反应结束后,应该继续通入一氧化碳直至玻璃管冷却至室温;
(3)氢氧化钠溶液能够吸收二氧化碳;
氧化铁中铁元素质量分数=$\frac{112}{160}$×100%×100%=70%;
根据实验现象可以判断相关方面的问题;
铁和稀盐酸反应生成氯化亚铁和氢气.
解答 解:(1)A区中,氧化铁和一氧化碳反应生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
B区中,碳燃烧生成二氧化碳,二氧化碳和碳反应生成一氧化碳,化学方程式分别为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;点燃\;}}{\;}$2CO;
(2)【实验与猜想】
①该小组的同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁;
②黑色固体粉末可能是四氧化三铁,或四氧化三铁和铁;
【得出结论】
假设产物是四氧化三铁,生成四氧化三铁质量为z,
3Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+3CO2,
480 464
6.0g z
$\frac{480}{6g}$=$\frac{464}{z}$
z=5.8g,
与假设符合,因此通过实验中获得的数据进行计算,得出黑色固体粉末为四氧化三铁;
【反思与评价】
②实验装置图(3)中采用虚线框内的装置,其作用有收集一氧化碳,吸收二氧化碳,故选:AB.
故答案为:(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(2)【实验与猜想】①氧化亚铁;
②为铁和四氧化三铁,全部为四氧化三铁;
【得出结论】四氧化三铁;
【反思与评价】②AB
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案| A. | 废旧电池随意丢弃 | |
| B. | 大量施用农药、化肥、增加农作物产量 | |
| C. | 废钢铁回炉冶炼成钢 | |
| D. | 加高烟囱,减少二氧化硫排放 |
| A. | 用活性炭除去冰箱内的异味 | B. | 氮气用作保护气 | ||
| C. | 用金属铜制作电线 | D. | 铁用来制铁锅 |